
| A.乙炔的燃烧热为1256kJ/mol |
| B.若转移10mol电子,则消耗2.5mol O2 |
| C.若生成2mol液态水,则△H=-2512kJ/mol |
| D.若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
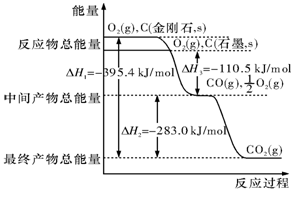
| A.等质量的硫蒸气和硫固体分别完全燃烧,反应的热效应ΔH1>ΔH2 |
| B.由C(石墨)→C(金刚石);ΔH=+1.9KJ/mol ,可知1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ,即金刚石比石墨稳定 |
| C.在101KPa时,2gH2完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l);ΔH=+285.8KJ/mol |
| D.放热及熵增加的反应,一定能自发进行 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH4(g)+2NO2(g)===N2(g)+CO2(g)+2H2O(l) ΔH=-867 kJ·mol-1 |
| B.CH4催化还原NOx为N2的过程中,若x=1.6,则转移电子3.2 mol |
| C.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ |
| D.若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移电子3.2 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 264 kJ·mol-1 | B.632 kJ·mol-1 | C.316 kJ·mol-1 | D.1 624 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是
2NH3(g)。当生成2molNH3时,放出热量为92kJ,在相同温度和压强下,向密闭容器中通入3mol H2和1mol N2,达到平衡时放出热量为Q,则下列关系式中正确的是| A.Q=92 kJ | B.Q< 92 kJ | C.Q> 92 kJ | D.Q<92×2 kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.2H2(g)+O2(g)===2H2O(l) ΔH1 |
| B.C(s)+O2(g)===CO(g) ΔH2 |
| C.CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH3 |
| D.C(s)+O2(g)===CO2(g) ΔH4 |
| 化学键 | P—P | P—O | O===O | P===O |
| 键能kJ/mol | 197 | 360 | 499 | x |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 化学键 | H—H | Cl—Cl | H—Cl |
| 生成(拆开)1mol化学键放出(吸收)的能量 | 436kJ | 243kJ | 431kJ |
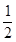 H2(g)+
H2(g)+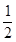 Cl2(g)="=HCl(g)" ;△H=-91.5kJ·mol-1
Cl2(g)="=HCl(g)" ;△H=-91.5kJ·mol-1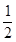 H2(g)+
H2(g)+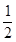 Cl2(g)="=HCl(g)" ;△H=+91.5kJ·mol-1
Cl2(g)="=HCl(g)" ;△H=+91.5kJ·mol-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com