
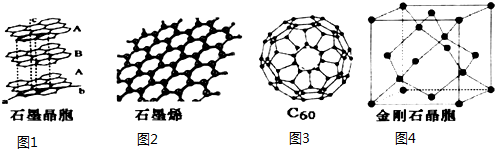
分析 (1)根据相似相溶原理分析C60易溶于有机溶剂的原因;
(2)该分子中甲基上C原子价层电子对个数是4且不含孤电子对,连接碳碳双键或碳氧双键的碳原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断C原子杂化方式;
(3)利用均摊法确定原子个数;
(4)石墨烯中每个碳原子被3个环共用,所以每个环上有2个碳原子,据此计算六元环个数;
a.在晶体中每一个碳原子与另三个碳原子间形成两个碳碳单键和一个碳碳双键;
b.石墨烯中每一个碳原子与另三个碳原子间形成两个碳碳单键和一个碳碳双键,所有碳原子可以处于同一个平面;
c.石墨中层与层之间存在分子间作用力;
(5)每个碳原子被3个环共用,则每个六元环中含有2个C原子,每个五元环中含有$\frac{5}{3}$个原子,据此计算六元环个数;
(6)金刚石晶胞中每个C原子和四个C原子形成共价键,所以C原子的配位数是4,该晶胞中C原子个数为4+6×$\frac{1}{2}$+8×$\frac{1}{8}$=8,设原子半径为xcm,两个原子中心的距离为晶胞体对角线的$\frac{1}{4}$,所以其体对角线距离为8xcm,则晶胞边长=$\sqrt{\frac{64}{3}}$xcm,晶胞体积=($\sqrt{\frac{64}{3}}$xcm)3,该晶胞中总的C原子体积=8×$\frac{4}{3}$πx3cm3.
解答 解:(1)根据相似相溶原理,C60易溶于有机溶剂,有机溶剂为分子晶体,则C60为分子晶体,故答案为:C60;
C60为分子晶体;
(2)该分子中甲基上C原子价层电子对个数是4且不含孤电子对,连接碳碳双键或碳氧双键的碳原子价层电子对个数是3且不含孤电子对,根据价层电子对互斥理论判断C原子杂化方式为sp3、sp2,故答案为:sp3、sp2;
(3)其结构为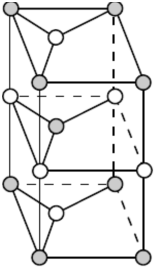 ,该晶胞中C原子个数=8×$\frac{1}{8}$+4×$\frac{1}{4}$+1+2×$\frac{1}{2}$=4,
,该晶胞中C原子个数=8×$\frac{1}{8}$+4×$\frac{1}{4}$+1+2×$\frac{1}{2}$=4,
故答案为:4;
(4)石墨烯中每个碳原子被3个环共用,所以每个环上有2个碳原子,六元环个数=$\frac{1}{2}$mol×NA/mol=0.5NA;
a.在晶体中每一个碳原子与另三个碳原子间形成两个碳碳单键和一个碳碳双键,故错误;
b.石墨烯中每一个碳原子与另三个碳原子间形成两个碳碳单键和一个碳碳双键,所有碳原子可以处于同一个平面
,故正确;
c.石墨中层与层之间存在分子间作用力,所以从石墨中剥离得到石墨烯需克服分子间作用力,故正确;
故选bc;
(5)每个碳原子被3个环共用,则每个六元环中含有2个C原子,每个五元环中含有$\frac{5}{3}$个原子,六元环个数=$\frac{60-12×\frac{5}{3}}{2}$=20,
故答案为:20;
(6)根据图知,金刚石晶胞中每个C原子和四个C原子形成共价键,所以C原子的配位数是4,该晶胞中C原子个数为4+6×$\frac{1}{2}$+8×$\frac{1}{8}$=8,设原子半径为xcm,两个原子中心的距离为晶胞体对角线的$\frac{1}{4}$,所以其体对角线距离为8xcm,则晶胞边长=$\sqrt{\frac{64}{3}}$xcm,晶胞体积=($\sqrt{\frac{64}{3}}$xcm)3,该晶胞中总的C原子体积=8×$\frac{4}{3}$πx3cm3,其空间利用率=$\frac{8×\frac{4}{3}×π×{x}^{3}c{m}^{3}}{(\sqrt{\frac{64}{3}}xcm)^{3}}×100%$=34.01%,
故答案为:4;34.01%.
点评 本题考查物质结构和性质,为高频考点,侧重考查学生分析计算及空间想象能力,涉及晶胞计算、原子杂化类型判断等知识点,难点是(3)(6)题的计算,知道晶胞空间利用率的计算方法,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | ①②④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
| A. | 增加Fe2O3固体可以提高CO的转化率 | |
| B. | 该反应的△H<0 | |
| C. | 减小容器体积既能提高反应速率又能提高平衡转化率 | |
| D. | 容器内气体密度恒定时,不能标志反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$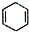 .下列有关说法不正确的是( )
.下列有关说法不正确的是( )| A. | D-A反应属于加成反应 | |
| B. | 2-甲基-1,3-丁二烯和丙烯发生D-A反应产物只有一种 | |
| C. | 如果要合成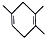 所用的原始原料可以是2,3-二甲基-1,3-丁二烯和丙炔 所用的原始原料可以是2,3-二甲基-1,3-丁二烯和丙炔 | |
| D. | D-A反应中的产物都可以使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硫有毒,严禁将其添加到任何食品和饮料中 | |
| B. | 饮食“镉大米”会影响骨骼和肾脏,镉元素属于重金属元素 | |
| C. | 使用增塑剂--邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶 | |
| D. | 面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 解释 |
| A | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 | Cl2和SO2均具有漂白性 |
| B | Fe与稀硝酸、稀硫酸反应均有气泡产生 | Fe与两种酸均发生置换反应 |
| C | 某物质燃烧后的产物既能使白色硫酸铜粉末变蓝,又能使澄清石灰水变浑浊 | 该物质可能是碳氢化合物 |
| D | 向某有机物的水溶液中加Na产生大量气体 | 该有机物中可能含有羟基或羧基 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在100℃、101 kPa条件下,1 mol液态水汽化时需要吸收40.69 kJ的热量,则H2O(g)═H2O(l)的△H=+40.69 kJ•mol-1 | |||||||||
| B. | 已知CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1,则CH4的燃烧热△H=-890.3 kJ | |||||||||
| C. | H2(g)+Br2(g)═2HBr(g)△H=-72 kJ•mol-1其他相关数据如表:
| |||||||||
| D. | 已知S(g)+O2(g)═SO2(s)△H1,S(g)+O2(g)═SO2(g)△H2,则△H2<△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结构片段为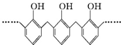 的高聚物,其单体是甲醛和苯酚 的高聚物,其单体是甲醛和苯酚 | |
| B. | 按系统命名法,有机物(CH3)2CHCH(CH2CH3)CH2CH2CH3命名为:2-甲基-3-乙基庚烷 | |
| C. | 由甘氨酸、丙氨酸形成的二肽有三种 | |
| D. | 乙烯和苯都能使溴水褪色,褪色原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
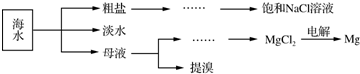
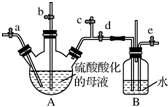
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com