
有200mL氯化镁和氯化铝的混合溶液,其中C(Mg2+)为0.2mol·L-1,C(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为
A. 80mL B. 40mL C. 72mL D. 128mL
科目:高中化学 来源:河北省2017届高三下学期三调考试理科综合化学试卷 题型:填空题
以某含铜矿石[主要成分是FeCuSi3O13(OH)4,含少量SiO2、CaCO3]为原料制备CuSO4·5H2O的流程如下:
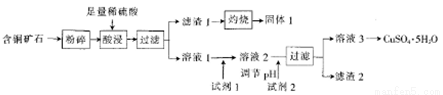
已知相关试剂成分和价格如下表所示:
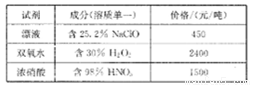
请回答下列问题:
(1)含铜矿石粉碎的目的是_______。
(2)酸浸后的溶液中除了Cu2+外,还含有的金属阳离子是_______。
(3)固体1溶于NaOH溶液的离子方程式为__________。
(4)结合题中信息可知:所选用的试剂1的名称为_______;加入该试剂时,发生反应的离子方程式为_________。
(5)试剂2 可以选择下列物成中的______。滤渣2中一定含有的物质为______(填化学式)。
A. Cu B.CuO C.Cu(OH)2 D.Fe
(6)CuSO4·5H2O用于电解精炼铜时,导线中通过9.632×103C的电量,测得阳极溶解的铜为16.0g。而电解质溶液(原溶液为1 L)中恰好无CuSO4,则理论上阴极质量增加_____g,原电解液中CuSO4的浓度为__ 。已知一个电子的电量为1.6×10-19C)
查看答案和解析>>
科目:高中化学 来源:2017届新疆乌鲁木齐地区高三第二次诊断性测验化学试卷(解析版) 题型:选择题
常温下向10mL0.1mol/L的HR溶液中逐渐滴入0.1mol/L的NH3·H2O溶液, 所得溶液pH及导电性变化如图。下列分析不正确的是
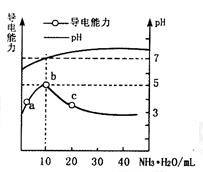
A.a~b点导电能力增强,说明HR为弱酸
B.b点溶液pH=7,说明NH4R没有水解
C.c点溶液存在c(NH4+)>c(R-)、c(OH-)>c(H+)
D.b~c任意点溶液均有c(H+)×c(OH-)=Kw=1.0×10-14
查看答案和解析>>
科目:高中化学 来源:南开中学2016-2017高三第四次月考理综化学试卷 题型:填空题
(16分) W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为 。
(2)W与Y可形成化合物W2Y,该化合物的电子式为 。
(3)X的硝酸盐水溶液显 性,用离子方程式解释原因: 。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为 。
(5)比较Y、Z气态氢化物的稳定性: > (用分子式表示)。
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是 > > > 。
(7)Z的最高价氧化物为无色液体,0.25 mol该物质与一定量水混合得到一种稀溶液,并放出QkJ的热量。写出该反应的热化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:计算题
社会实践活动中,课外兴趣小组对某钢铁厂的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息。下面请你根据他们的实验帮助计算回答:
取该厂的某钢样粉末28.36 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3 g白色沉淀。
(1)计算此钢样粉末中铁和碳的质量之比。
(2)再取三份不同质量的钢样粉末分别加到50 g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2 g H2的体积为22.4 L)
实验序号 | Ⅰ | Ⅱ | Ⅲ |
加入钢样粉末的质量 / g | 2.836 | 5.672 | 8.508 |
生成气体的体积(标准状况)/ L | 1.12 | 2.24 | 2.80 |
请根据表中数据计算硫酸中H2SO4的质量分数。
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少? (用含m的代数式表示)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:选择题
下列各组化合物中,化学键类型完全相同的时( )
A.CaCl2 和 Na2S B.Na2O 和Na2O2
C.CO2 和 CaO D.HCl 和NaOH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是( )
A. CO2的比例模型: B. 氢氧根离子的电子式:
B. 氢氧根离子的电子式: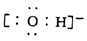
C. 氯原子的结构示意图: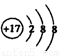 D. 中子数为146,质子数为92的铀(U)原子
D. 中子数为146,质子数为92的铀(U)原子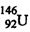
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南师范大学附属中学高一3月月考化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分元素,用元素符号或化学式回答下列问题:
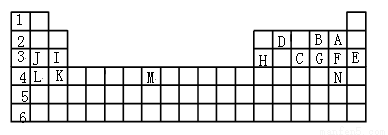
① 表中用字母标出的14种元素中,化学性质最不活泼的是________,主族元素中金属性最强的是_______,常温下单质为液态的非金属元素是_______;属于过渡元素的是_________。
②C、G、F气态氢化物的稳定性顺序是______________________ 。
③第三周期中原子半径最小的元素是_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高二上学期期末检测化学试卷(解析版) 题型:简答题
25 ℃时,几种弱酸的电离常数如下:
弱酸化学式 | HNO2 | CH3COOH | HCN | H2CO3 |
电离常数 | 5.1×10-4 | 1.8×10-5 | 6.2×10-10 | K1=4.4×10-7 K2=4.7×10-11 |
(1)根据上表数据填空:
①物质的量浓度相同的四种酸,其pH由大到小的顺序是___________ (用化学式填写)。
②分别向等体积、相同pH的HCl溶液和CH3COOH溶液中加入足量的Zn粉,反应刚开始时产生H2的速率:v(HCl)______v(CH3COOH)(填“=”、“>”或“<”下同),反应完全后,所得氢气的质量:m(H2)盐酸_______m(H2)醋酸。
③将0.2 mol/L HCN溶液与0.1 mol/L Na2CO3溶液等体积混合,发生反应的化学方程式为___________________________。
(2)体积均为10 mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程中溶液pH变化如图所示。稀释后,HX溶液中水电离的c(H+) ___醋酸溶液中水电离的c(H+) ;电离常数Ka(HX)___Ka(CH3COOH)(填“>”、“=”或“<”)。
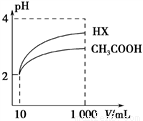
(3)CO32- 、 NO2- 、CN-、CH3COO-结合H+的能力由强到弱的顺序为_______________________(用离子符号表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com