
【题目】有机物C5H11OH为饱和一元醇,其可能的结构共有( )
A.3种
B.5种
C.8种
D.9种
 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
【题目】下图是实验室制取Na2S2O3·5H2O的装置图(略去部分夹持仪器)。
已知:Na2SO3 +S![]() Na2S2O3
Na2S2O3
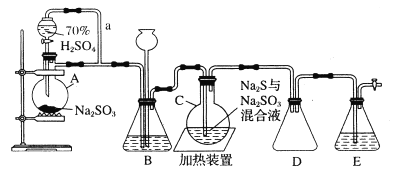
按要求回答下列问题:
(1)仪器A的名称是___________________。
(2)分液漏斗中用70%较浓硫酸的理由是___________________。
(3)装置C中生成S的离子反应方程式是___________________。
(4)E是SO2的尾气处理装置,则装置D的作用是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.1 mol CH4的质量为16 g/mol
B.N2的摩尔质量为28g
C.0.5mol O2中含O2分子约3.01×1023个
D.标准状况下,1 molH2O的体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离子方程式错误的是
A.NaHCO3=Na++HCO3-B.NaHSO4=Na++H++SO42-
C.KClO3=K++Cl-+3O2-D.H2SO4=2H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在使用分液漏斗进行分液时,正确的操作是( )
A.上层液体经漏斗下口放出
B.分离液体时,将漏斗拿在手上进行分离
C.分离液体时,使分液漏斗玻璃塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液漏斗下面的活塞拧开
D.分液漏斗中盛装的是液体,振荡后不必打开活塞把气体放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A. NH3、O2、NO、H2O(g)同时存在时,则反应达到化学平衡状态
B. 单位时间内生成x mol NO,同时消耗x mol NH3时,说明反应达到化学平衡状态
C. 达到化学平衡状态时,若增大容器体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率关系是3v正(NH3)=2v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在高温高压下碳氧化物具有极高的化学活性,能与多种单质或化合物反应。
(1)一定条件下,CO与H2 可合成甲烷,反应方程式为:CO(g)+3H2(g) ![]() CH4(g)+ H2O(g)
CH4(g)+ H2O(g)
①一定条件下,该反应能够自发进行的原因是_________
②已知H2(g)、CO(g)和CH4(g)的燃烧热分别为285.8kJ/mol 283.0kJ/mol和890.0kJ/mol。
写出CO 与H2 反应生成CH4 和CO2 的热化学方程式:_____________。
(2)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ: CO (g) +2H2 (g) ![]() CH3OH (g)
CH3OH (g)
反应Ⅱ: CO2 (g) +3H2 (g) ![]() CH3OH (g) +H2O (g)
CH3OH (g) +H2O (g)
①在以上制备甲醇的两个反应中:反应Ⅰ优于反应Ⅱ,原因为______________。
②一定温度下,在体积可变的密闭容器中加入4molH2和一定量的CO发生反应Ⅰ,开始时容器体积为2L,CO 和CH3OH (g) 的浓度随时可变化如图。10min 达到平衡,则反应1的化学平衡常数为____________。
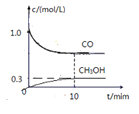
③恒温恒容条件下,在密闭容器中等物质的量的通入CO2 和H2, 下列描述能说明反应Ⅱ已经达到平衡状态的是___。(填标号)
A.容器内CO2的体积分数不再变化
B.当CO2和H2转化率的比值不再变化
C.单位时间CH3OH分子断裂5NA个共价键,同时断裂3NA个H-H键
D.容器内混合气体的平均相对分子质量为34.5,且保持不变
(3)甲烷碱性燃料电池装置如图所示(开始时两边溶液质量相等),用电器为惰性电极电解装置,其原理是:通电后,将Co2+氧化成Co3+,进而彻底氧化CN-为无害气体使废水得以净化。
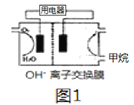
①当除去1molCN-时,图1两边质量差为__________g.
②负极电极反应式为__________.
(4)工业上可通过甲醇羰基化法制取甲酸甲酯,反应方程式为:CH3OH(g)+CO(g) ![]() HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
HCOOCH3(g) ΔH=-29.1KJ/mol,科研人员对该反应进行了研究.部分研究结果如下:
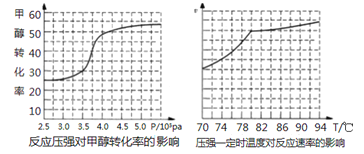
①从反应压强对甲醇转化率的影响“效率”看,工业制取甲酸甲酯应选择的压强是_____。
②实际工业生产中采用的温度是80℃,其理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)是一种高效的饮用水处理剂,工业上可由下列方法制得:Fe2O3+3Na2O2![]() 2Na2FeO4+Na2O,关于该反应说法正确的是
2Na2FeO4+Na2O,关于该反应说法正确的是
A. Fe2O3可以通过铁丝在氧气中燃烧制得
B. 反应中Na2O2是氧化剂
C. 生成1 mol Na2FeO4,有6 mol电子转移
D. 在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌,又能在处理水时产生胶体净水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com