
| A. | 84% | B. | 42% | C. | 53% | D. | 67% |
分析 NaHCO3 固体加热发生2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,结合质量的变化利用差量法解答该题.
解答 解:设有xg NaHCO3分解,则
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O△m
2×84g 106g 62g
xg 20g-13.8g=6.2g
x=$\frac{168×6.2}{62}$=16.8,
则NaHCO3 的分解百分率为$\frac{16.8}{20}×100%$=84%.
故选A.
点评 本题是考查化学方程式的书写及方程式的计算,为高频考点,注意把握差量法在方程式计算中的应用,题目培养学生分解决问题的能力和计算能力,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
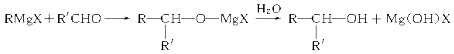
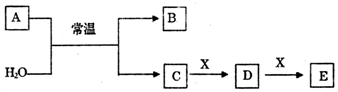
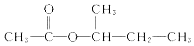 )的流程如下(部分反应物及反应条件没有列出),A主要来源于石油裂解气,A的产量常作为衡量石油化工水平的标志.
)的流程如下(部分反应物及反应条件没有列出),A主要来源于石油裂解气,A的产量常作为衡量石油化工水平的标志.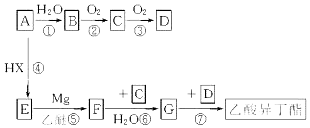
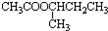 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46g NO2和N2O4的混合气体中含有的原子个数为3NA | |
| B. | 1 mol Na2O2与水完全反应时转移电子数为2NA | |
| C. | 标准状况下,2.24L庚烷含有的分子数为0.1NA | |
| D. | 1 mol Na2O2中含有的阴离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A | Fe(OH )3 胶体通电后 | 阴极区红褐色加深 | Fe(OH)3胶体带 正电 |
| B | 将铜粉加入 1.0mol•L-1 的Fe2(SO4)3溶液中 | 溶液变蓝,有黑色固体出现 | 金属Fe比Cu活 泼 |
| C | 用坩埚钳夹住用砂纸 仔细打磨过的铝箔在 酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点比 较低 |
| D | 向盛有少量浓硝酸、 稀硝酸的两支试管中 分别加入一片大小相 同的铜片 | 浓硝酸中铜片很快开始溶解,并放出 红棕色气体;稀硝酸中过一会铜片表 面才出现无色气体,气体遇空气变红 棕色 | 浓硝酸氧化性强 于稀硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3的水解:HCO3-+H2O?H3O++CO32- | |
| B. | 醋酸的电离:CH3COOH═CH3COO-+H+ | |
| C. | 碳酸钙的溶解平衡:CaCO3(s)?Ca2+(aq)+CO32-(aq) | |
| D. | H2的燃烧热为285.8 kJ/mol,则表示H2燃烧热的热化学方程式为:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||||
| Z | Y | M | N |
| A. | N的含氧酸一定是强酸 | B. | 单质Z比单质Y活泼 | ||
| C. | X的原子半径比Y的小 | D. | X和M的原子序数相差10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.0008mol/L | B. | 0.00125mol/L | C. | 0.8mol/L | D. | 1.25mo/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入Ba(NO3)2溶液,再滴加稀盐酸,出现白色沉淀且不溶解,则原溶液中可能含有SO32- | |
| B. | 某气体使湿润的蓝色试纸变红,则该气体一定是酸性氧化物 | |
| C. | 乙醇中混有乙酸,加入氢氧化钠后蒸馏即得纯净的乙醇 | |
| D. | 在分液漏斗中加入溴水,然后加入适量CCl4,振荡后静置,溴可萃取到CCl4中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com