
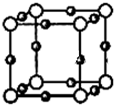
 ,分子中含有2个C-H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;
,分子中含有2个C-H键、1个C=O键,单键为σ键,双键中具有1个σ键、1π键,故分子中σ键和π键数目比为3:1;| 1 |
| 4 |
| 1 |
| 8 |


科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子核外电子排布式为1s2的元素与原子核外电子排布式为1s22s2的元素化学性质相似 |
| B.Fe3+的最外层电子排布式为:3s23p63d5 |
C.基态铜原子的价电子排布图: |
D.基态碳原子的价电子排布图: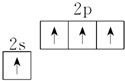 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3p能级有一个空轨道的基态原子和核外电子的排布为1s22s22p63s23p2的原子 |
| B.2p能级无空轨道,且有一个未成对电子基态原子和原子的最外层电子排布为2s22p5的原子 |
| C.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p5的原子 |
| D.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p63d64s2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子核外的电子象云雾一样笼罩在原子核周围,故称电子云 |
| B.s能级的原子轨道呈球形,处在该轨道上的电子只能在球壳内运动 |
| C.p能级的原子轨道呈纺锤形,随着电子层的增加,p能级原子轨道也在增多 |
| D.与s原子轨道的电子相同,p原子轨道电子的平均能量随能层的增大而增加 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | A | B | C | D |
| 性质或 结构信息 | 其单质和化合物的焰色均为黄色 | 其氢化物的水溶液能腐蚀玻璃 | 其单质在空气中体积含量最多 | 地壳中含量最多的金属元素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com