
分析 (1)第三周期中,化学性质最不活泼的元素是稀有气体Ar,可用于制半导体材料的元素是Si,非金属性越强,最高价氧化物的水化物酸性越强;
(2)Fe元素在元素周期表中的位置是第四周期第VIII族;
(3)根据烷烃命名原则:
①长-----选最长碳链为主链;
②多-----遇等长碳链时,支链最多为主链;
③近-----离支链最近一端编号;
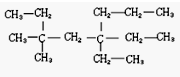
④小-----支链编号之和最小,看下面结构简式,从右端或左端看,均符合“近-----离支链最近一端编号”的原则;
⑤简-----两取代基距离主链两端等距离时,从简单取代基开始编号.如取代基不同,就把简单的写在前面,复杂的写在后面;
(4)根据烷烃命名原则书写;
(5)主链上含有5个碳原子,分子中共有7个碳原子的烷烃,则可能含有1个支链为-CH2CH3,可能含有2个-CH3,据此书写符合条件的结构进行解答.
解答 解:(1)第三周期中,化学性质最不活泼的元素是稀有气体Ar,可用于制半导体材料的元素是Si,第三周期非金属性最强的是氯,最高价氧化物的水化物酸性最强的是高氯酸,
故答案为:Ar;Si;HClO4;
(2)Fe元素在元素周期表中的位置是第四周期第VIII族,
故答案为:第四周期第VIII;
(3) 最长链上碳的个数为8,则称为辛烷,3号碳有2个甲基,5号碳上有2个乙基,则名称为:3,3-二甲基-5,5-二乙基辛烷,
最长链上碳的个数为8,则称为辛烷,3号碳有2个甲基,5号碳上有2个乙基,则名称为:3,3-二甲基-5,5-二乙基辛烷,
故答案为:3,3-二甲基-5,5-二乙基辛烷;
(4)2,2-二甲基-4-乙基庚烷,最长的主链含有7个C原子,2个甲基处于2号碳原子上,乙基处于4号碳上,其结构简式为:CH3C(CH3)2CH2C(CH2CH3)2CH2CH2CH3,5,5-二甲基-3-乙基辛烷,最长的主链含有8个C原子,2个甲基处于5号碳原子上,乙基处于3号碳上,其结构简式为:CH3CH2CH(CH2CH3)CH2C(CH3)2CH2CH2CH3,
故答案为:CH3C(CH3)2CH2C(CH2CH3)2CH2CH2CH3;CH3CH2CH(CH2CH3)CH2C(CH3)2CH2CH2CH3;
(5)主链上含有5个碳原子,分子中共有7个碳原子的烷烃,若含有1个支链为-CH2CH3,则为CH3CH2CH2(CH2CH3)2,只有1种,
若含有2个-CH3,则为:CH3CH2C(CH3)2CH2CH3,CH3CH2CH2C(CH3)2CH3,CH3CH2CH(CH3)CH(CH3)CH3,CH3CH(CH3)CH2CH(CH3)CH3,有4种,故共有5种,
故答案为:5.
点评 本题考查元素周期表的结构及其应用、有机化合物的命名、同分导构体的书写,是组合题型,注意基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2 溶液中滴入过量NaOH溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向NaAlO2 溶液中通入过量的 CO2:CO2+2H2O+A1O2-═Al(OH)3↓+HCO3- | |
| C. | 0.01mol/L NH4Al(SO4)2 溶液与 0.02mol/L Ba(OH)2 溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| D. | 向Ca(ClO)2 溶液中通入过量的 SO2:C1O-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑤⑥ | B. | ①③④⑥ | C. | ②④⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
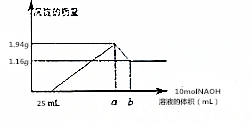 将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题:
将一定质量的镁和铝合金粉末溶解于50mL某浓度的盐酸中,等合金全部溶解后,再向其中加入某浓度的NaOH溶液,在此过程中,产生沉淀的质量与所需要消耗NaOH溶液的体积关系如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I-Fe3+ Na+ | B. | Al3+Ba2+HCO3- | C. | K+Na+CO32- | D. | NH4+K+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
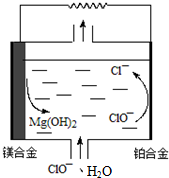
| A. | Mg-Li合金比传统的Mg-Al合金具有更高的比能量 | |
| B. | 铂合金的电极反应:ClO-+H2O═Cl-+2OH--2e-,OH-向镁合金电极迁移 | |
| C. | 该电池镁合金会发生自身腐蚀产生氢气,使电极利用率降低 | |
| D. | 把电解质换成H2O2、H2SO4和NaCl的混合溶液,工作时H2O2将参与电极反应,其电极反应为:2H2O2-2e-═O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若温度不变,将容器的体积增大一倍,此时的SO2浓度变为原来的0.5倍 | |
| B. | 若平衡时SO2、O2的转化率相等,说明反应开始时,两者的物质的量这比为2:1 | |
| C. | 若从平衡体系中分离出SO3,则有利于提高SO2的转化率和加快正反应速率 | |
| D. | 平衡状态时SO2、O2、SO3的物质的量之比一定为2:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生铁在潮湿的空气中易发生化学腐蚀而锈蚀 | |
| B. | 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化 | |
| C. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| D. | 在米汤中加入食盐,可以检验食盐中是否加碘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com