
【题目】随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
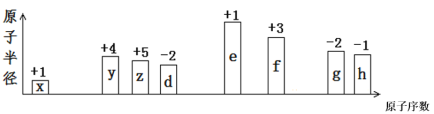
根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________________。
(2)比较d、e常见离子的半径大小(用化学式表示)___________________;
(3)z的简单氢化物与z的最高价氧化物的水化物形成的化合物中化学键类型为:_______________________。
(4)元素y的一种同位素可用于测定文物年代,这种同位素原子符号为___________。
(5)元素g与元素h相比,非金属性较强的是_________(用元素符号表示),下列表述中能证明这一事实的是_________(填序号)。
a.常温下g的单质和h的单质状态不同
b.h的氢化物比g的氢化物稳定
c.一定条件下g和h的单质都能与氢氧化钠溶液反应
d.g、h最高价氧化物对应水化物的酸性前者弱于后者
(6)x、e反应可生成离子化合物ex。
①写出化合物ex的电子式__________________。
②将少量ex投入水中,剧烈反应,得到x单质。
写出反应的化学方程式:_____________________________________________;
【答案】第三周期 ⅢA族 O2->Na+ 离子键 共价键 ![]() C Cl bd
C Cl bd ![]() NaH+H2O=NaOH+H2↑
NaH+H2O=NaOH+H2↑
【解析】
推此题元素需运用元素周期律知识:同周期元素原子半径逐渐减小,最高正价逐渐增大,最低负价绝对值逐渐减小。依此规律并结合图表可推出图中所列各种元素:x原子半径最小,最高+1价,是H;y、z、d属第二周期元素,根据最高或最低化合价分别为+4、+5、-2,可知分别是C、N、O;e、f、g、h为第三周期元素,根据其最高正价或最低负价分别为+1、+3、-2、-1可推出它们分别是Na、Al、S、Cl。在此基础上,结合元素化合物知识,可对各小题进行解答。
(1)f是Al,位于元素周期表中第三周期、第IIIA族,所以答案为:第三周期 IIIA族。
(2)d、e分别是O、Na,常见离子分别是O2-、Na+,它们均为10电子粒子,O的核电荷数比Na的小,所以半径关系是:O2->Na+。答案为:O2->Na+。
(3)z是N,简单氢化物(NH3)和最高价氧化物的水化物(HNO3)形成的NH4NO3是离子化合物,含离子键;![]() 中氮氢键、
中氮氢键、![]() 中的氮氧键均为共价键,所以答案为:离子键 共价键。
中的氮氧键均为共价键,所以答案为:离子键 共价键。
(4)y是C,其同位素C-14可用于测定文物年代,所以答案为:![]() C 。
C 。
(5)g是S,h是Cl,同周期主族元素原子序数越大非金属性越强,所以Cl非金属性比S强;单质的状态不能用于非金属性的比较,a错;非金属性越强氢化物越稳定,b对;与氢氧化钠溶液反应是共同的性质,不能用于区别非金属性,c错;最高价氧化物对应水化物的酸性越强,非金属性越强,d对。故答案为:Cl; bd。
(6)x、e分别是H、Na,形成的离子化合物是NaH,①NaH是由Na+和H-构成,所以电子式为![]()
;②-1价氢还原性强,NaH投入水中,所含负一价氢能与水中正一价氢发生归中反应生成氢气:NaH+H2O=NaOH+H2↑。故答案为:![]() NaH+H2O=NaOH+H2↑。
NaH+H2O=NaOH+H2↑。


科目:高中化学 来源: 题型:
【题目】如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出。常温下X是固体,B和G是液体,其余均为气体。根据下图关系推断:

(1)写出化学式:X_______,A________,B_______。
(2)实验室收集气体D和F的方法依次是_______法、________法。
(3)写出C→E的化学方程式:____________。
(4)请写出A与E反应生成D的化学方程式:_______________
(5)检验物质A的方法和现象是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在新制氯水中存在多种分子和离子,下列实验现象和结论一致且正确的是( )
A. 新制氯水使红玫瑰变为白玫瑰,说明有Cl2
B. 加入石蕊溶液,溶液变红,说明该溶液一定不含HClO
C. 将KHCO3固体加入新制的氯水中,有气泡产生,说明有HClO
D. 光照新制氯水有气泡逸出,该气体一定是O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.已知2C+SiO2![]() Si+2CO↑,说明Si的非金属性比C强
Si+2CO↑,说明Si的非金属性比C强
B.电子层数越多,原子半径一定越大
C.碱金属元素都能与氧气反应生成过氧化物
D.单质中不可能含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的单质及X与Y形成的化合物能按下图所示的关系发生转化(其中m、n均为正整数,且m≠n)。下列说法正确的是
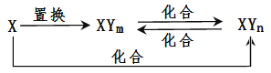
A.X一定是多价态金属元素
B.X一定是非金属元素
C.XYm与XYn的相互转化属于可逆反应
D.X、Y均为非金属元素,也可以实现上述转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】α1和α2分别为A在甲、乙两个恒容容器中平衡体系A(g)+B(g)![]() C(g)和2A(g)
C(g)和2A(g)![]() B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
A. α1、α2均减小B. α1、α2均增大C. α1减小,α2增大D. α1增大,α2减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
A. 图 表示温度对平衡的影响,且甲温度较高
表示温度对平衡的影响,且甲温度较高
B. 图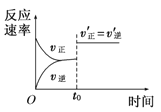 表示t0时刻恒容充入He(g)
表示t0时刻恒容充入He(g)
C. 图 表示t0时刻增大O2的浓度对反应速率的影响
表示t0时刻增大O2的浓度对反应速率的影响
D. 图 中a点v正 > v逆
中a点v正 > v逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.《吕氏春秋》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特性
B.工业生产玻璃和水泥使用到的共同原料有![]()
C.碳纳米点是一种直径小于10nm的材料。由它作为分散质形成的分散系叫做胶体
D.天然气是一种清洁的化石燃料,作为化工原料它主要用于合成氨和甲醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中两种溶液间的反应,均可用同一离子方程式表示的是( )
A.HCl+Na2CO3、HCl+NaHCO3B.BaCl2+Na2SO4、Ba(OH)2+H2SO4
C.石灰石与硝酸、石灰石与盐酸D.KOH+HCl、Ba(OH)2+H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com