
【题目】为了除去KCl溶液中少量的MgCl2、MgSO4,从稀盐酸、Na2CO3、Ba(NO3)2、K2CO3、Ba(OH)2溶液中,选择A、B、C 3种试剂,按图中的实验步骤进行操作:
![]()

![]()
![]()
![]()
![]()
(1)3种试剂的化学式:A________B________C________
(2)加过量A的原因是___________________,有关反应的化学方程式_______________________、___________________________。
(3)加过量B的原因是____________________,有关反应的化学方程式为_____________________、___________________________
【答案】 Ba(OH)2 K2CO3 稀盐酸 为了除尽Mg2+、SO42- MgCl2+Ba(OH)2===BaCl2+Mg(OH)2↓ MgSO4+Ba(OH)2===BaSO4↓+Mg(OH)2↓ 为了除尽过量的Ba2+ Ba(OH)2+K2CO3=2KOH+BaCO3↓ BaCl2+K2CO3===BaCO3↓+2KCl
【解析】试题分析:除去KCl溶液中少量的MgCl2、MgSO4,为防止引入杂质,Na2CO3和Ba(NO3)2是不能使用的。应先加入稍过量的Ba(OH)2,把MgCl2和MgSO4完全沉淀,然后再加入稍过量的K2CO3除去过量的Ba(OH)2,过滤后,向滤液中加入稀盐酸除去过量的K2CO3。
(1)3种试剂的化学式:A、Ba(OH)2,B、K2CO3,C、稀盐酸。
(2)加过量Ba(OH)2的原因是为了除尽Mg2+、SO42-,有关反应的化学方程式MgCl2+Ba(OH)2===BaCl2+Mg(OH)2↓、MgSO4+Ba(OH)2===BaSO4↓+Mg(OH)2↓。
(3)加过量K2CO3的原因是为了除尽过量的Ba2+,有关反应的化学方程式为Ba(OH)2+K2CO3=2KOH+BaCO3↓、BaCl2+K2CO3===BaCO3↓+2KCl


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验探究:探究碳、硅元素的非金属性的相对强弱。根据要求完成 下列各小题。
(1)实验装置:
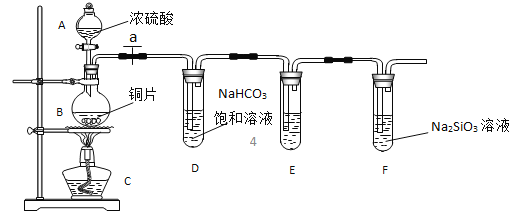
填写所示仪器名称 A_________B________________________
(2)实验步骤:
连接仪器、_____________、加药品后,打开 a、然后滴入浓硫酸,加热
(3)问题探究:(已知酸性强弱:亚硫酸 >碳酸)
①铜与浓硫酸反应的化学方程式是________________________________;装置E中足量酸性KMnO4溶液的作用是_____________________________;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是____________________________;
③依据试管 D 中的实验现象,能否证明硫元素的非金属性强于碳元素的非金属性___(填 “能”或“否”),试管 D 中发生反应的离子方程式是______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是铁的一种重要化合物,是一种新型、高效、多功能水处理剂。一种湿法制备高铁酸钾的工艺流程如下图所示:
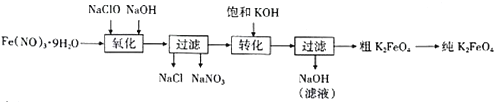
已知高铁酸钾的部分性质如下:
① 热稳定性差,溶液的pH对其稳定性的影响也很大;即在低温、碱性环境中稳定,高温、中性和酸性条件下不稳定。
② 在水中溶解度大,难溶于无水乙醇等有机溶剂。
③ 具有强氧化性,能氧化烃、80%以下的乙醇溶液等物质。
回答下列问题:
(1)该生产工艺应在温度_____(填“较高”或“较低”)的情况下进行。
(2)上述氧化过程中,发生反应的离了方程式为_______。
(3)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾
① 加入饱和KOH溶液的目的是:______。
② 由以上信息可知:Ksp(K2FeO4)______Ksp(Na2FeO4)(填“大于”或“小于”)。
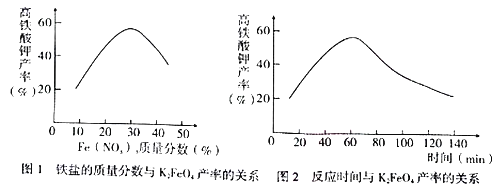
(4)实验测得铁盐溶液的质量分数、反应时间与K2FeO4产率的实验数据分别如下图l、图2所示。为了获取更多的高铁酸钾,铁盐的质量分数应控制在______附近、反应时间应控制在______。
(5)粗K2FeO4→纯K2FeO4包括重结晶、过滤、洗涤、干燥几个步骤。洗涤、干燥的目的是脱碱、脱水,洗涤时最好用______洗涤。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质或离子检验的叙述正确的是( )
A. 往品红溶液中通入气体,红色褪去,证明气体一定是二氧化硫
B. 气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C. 加入氯化钡溶液生成沉淀,再加入盐酸沉淀不溶解证明一定含有硫酸根
D. 将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组利用下图装置进行碱式碳酸钴[Cox(OH)y(CO3)z]的化学组成测定的探究实验,图中铁架台等装置已略去,粗黑线表示乳胶管。

已知碱式碳酸钴受热时按右式分解:碱式碳酸钴![]() 钴的氧化物+CO2↑+H2O↑。
钴的氧化物+CO2↑+H2O↑。
回答下列问题:
(l)按如图所示装置组装好仪器,在装药品前,应先进行的操作是_______。
(2)称取3.65g样品置于硬质玻璃管内;打开活塞a,缓缓通入空气数分钟,关闭活塞a;加热硬质玻璃管,当丙装置中不再有气泡产生时,停止加热;又打开活塞a,再缓缓通入空气数分钟。两次通入空气的目的不同,第一次的目的是将装置中含二氧化碳和水蒸气的空气排尽,第二次的目的是______。
(3)通过正确实验测得丙、丁装置增重分别为0.36g、0.88g,则该碱式碳酸钴的化学式为______。
(4)甲装置中X试剂是______(填标号)。
a.浓硫酸 b.水氯化钙 c.五氧化二磷粉末 d.碱石灰
(5)若去掉戊装置,会使x的值______(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL0.5mol L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是

A. 由水电离出的c(H+):C点>B点
B. 醋酸的电离平衡常数:B点> A点
C. 从A点到B点,混合溶液中可能存在:c( CH3COO-) = c(Na+)
D. C 点混合溶液中一定存在:c(Na+) =2c(CH3COO-) +2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加徳罗常数的值,下列说法中正确的是
A. 8.0g Cu2S和CuO的混合物中含有铜原子数为0.1 NA
B. 常温常压下,36g 18O2中所含的中子数为16 NA
C. 电解饱和食盐水时,阳极上生成22.4L气体时转移的电子数为2 NA
D. 标准状况下,11.2LH2O中含有H—O键的数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com