
【题目】姜黄素有抗氧化、保肝护肝、抑制肿瘤生长等功能。它的结构简式如图所示
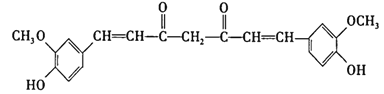
已知: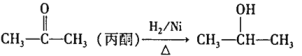
下列有关姜黄素的说法正确的是
A. 姜黄素在一定条件下能发生水解、加成、氧化反应
B. 1个姜黄素分子一定有15个原子共平面
C. 1mol姜黄素在镍(Ni)、加热条件下最多10molH2发生加成反应
D. 姜黄素的分子式为C21H18O6
【答案】C
【解析】姜黄素分子结构具有对称性,其中含有醚键、酚羟基、碳碳双键、羰基官能团,结合酚和烯烃的性质分析解答。
A. 姜黄素分子结构中没有能够水解的官能团,不能发生水解反应,故A错误;B.苯环、碳碳双键和羰基均为平面结构,但碳碳单键可以旋转,1个姜黄素分子中的碳原子可能都在同一平面上,但不一定有15个原子共平面,故B错误;C. 苯环、碳碳双键和羰基都能与氢气加成,1mol姜黄素在镍(Ni)、加热条件下最多10molH2发生加成反应,故C正确;D. 根据姜黄素的结构简式可知,姜黄素的分子式为C21H20O6,故D错误;故选C。
点晴:本题考查有机物的结构和性质,掌握官能团的结构和性质是解题的关键。本题的易错点为B,要根据常见的基本物质(甲烷、乙烯、乙炔、苯、甲醛)的结构分析解答,同时注意碳碳单键是可以旋转的,该分子中最少7个碳原子,最多21个碳原子共平面。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包Na2O2样品是否已经变质:取少量样品,将其溶解,加入__________溶液,充分振荡后有白色沉淀,证明Na2O2已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了m g样品,并设计用下图装置来测定过氧化钠的质量分数。
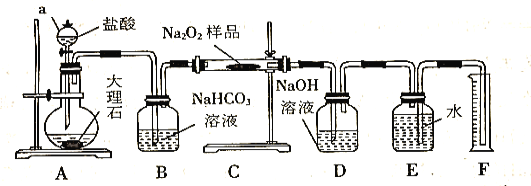
①装置D的作用是_________________________________;
②将仪器连接好以后,必须进行的第一步操作是_________________________________;
③写出装置C中发生主要反应的化学方程式_________________________________;
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是_______________(填序号);
a.读取气体体积前,需冷却到室温
b.调整量筒使E、F内液面高度相同
c.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成标准状况下氧气的体积为VmL,则样品中过氧化钠的质量分数为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体.若As2S3和SnCl2正好完全反应,As2S3和HCl的物质的量之比为________。写出化学方程式并用双线桥法标出电子转移_______________________________________________。
(2)上述反应中的氧化剂是________,反应产生的气体可用________吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O
若生成2 mol H3AsO4,则反应中转移电子的物质的量为________。若将该反应设计成一原电池,则NO2应该在________(填“正极”或“负极”)附近逸出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式不正确的是
A.Fe3O4与HI反应的离子方程式为:Fe3O4+8H++2I—=3Fe2++I2+4H2O
B.用稀H2SO4除去铜绿:4H++Cu2(OH)2CO3=2Cu2++CO2↑+3H2O
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀:
2Ba2++Al3++2SO42—+4OH—=AlO2—+2H2O+2BaSO4↓
D.少量Ca(OH)2溶液与NaHCO3混合:Ca2++2OH—+2HCO3—=CaCO3↓+2H2O+CO32—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出下列化学方程式
(1)乙炔与氯化氢按物质的量比1:1反应_____________________________________
(2)苯与浓硝酸、浓硫酸的混合酸共热_____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向50 mL 0.018 mol/L的AgNO3溶液中加入50 mL 0.02 mol/L的盐酸生成沉淀。已知:Ksp(AgCl)=1.8×10-10mol2·L-2,则生成沉淀后的溶液中c(Ag+)与pH分别为
A. 1.8×10-7mol/L,2 B. 1×10-7mol/L,2 C. 1.8×10-7mol/L,3 D. 1×10-7mol/L,3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1 molL-1、体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=l00mL,Va、Vb与混合液的pH的关系如图所示。 下列说法正确的是

A. Ka(HA)=10-6mol·L-1
B. b点时,c(B+)=c(A-)=c(H+)=c(OH-)
C. c点时,  随温度升高而减小
随温度升高而减小
D. a→c过程中水的电离程度始终增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com