
 利用H2S废气制取氢气来的方法有多种
利用H2S废气制取氢气来的方法有多种
①高温热分解法
已知:H2S(g)  H2(g)+
H2(g)+ 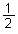 S2(g)
S2(g)
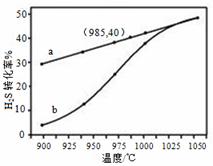
在恒温密闭容器中,控制不同温度进行H2S分解实验。以H2S起始浓度均为c mol·L-1测定H2S的转化率,结果见右图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。据图计算985℃时H2S按上述反应分解的平衡常数K=___ ___;说明随温度的升高,曲线b向曲线a逼近的原因:
 ②电化学法
②电化学法
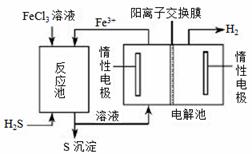
该法制氢过程的示意图如右。反应池中反应物的流向采用气、液逆流方式,其目的是 ;反应池中发生反应的化学方程式为 。反应后的溶液进入电解池,电解总反应的离子方程式为 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
以熔融Li2CO3和K2CO3为电解质,天然气经重整催化作用提供反应气的燃料电池如右图。下列说法正确的是
A.以此电池为电源电解精炼铜,当有0.1 mol e- 转移时,有3.2 g铜溶解
B.若以甲烷为燃料气时负极极反应式:
CH4+5O2--8e-=CO32-+2H2O
C.该电池使用过程中需补充Li2CO3和K2CO3
D.空气极发生的电极反应式为
O2+4e-+2CO2===2CO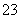
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象或应用不能用胶体的知识解释的是( )
A.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.土壤表面积巨大且一般带负电,能吸收NH4+等营养离子,使土壤具有保肥能力
C.水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
D.氯化铝溶液中加入碳酸钠溶液会出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作正确且能达到预期目的的是
| 编号 | 实验目的 | 操作 |
| ① | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| ② | 欲证明CH2==CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| ③ | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| ④ | 证明SO2具有漂白性 | 将SO2通入酸性KMnO4溶液中 |
| ⑤ | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
| ⑥ | 确定碳和硅两元素非金属性强弱 | 测同温同浓度Na2CO3和Na2SiO3水溶液的pH |
A.①④⑤ B.②③⑤ C.①⑤⑥ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
 煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料。试用所学知识,解答下列问题:
(1)煤的转化技术包括煤的气化技术和液化技术。煤的液化技术又分为________和________。
(2)在煤燃烧前需对煤进行脱硫处理。煤的某种
 脱硫技术的原理为FeS2 Fe2++SO42—
脱硫技术的原理为FeS2 Fe2++SO42—
Fe3+这种脱硫技术称为微生物脱硫技术。该技术的第一步反应的离子方程式为_____________________________,
第二步反应的离子方程式为____________________。
(3)工业煤干馏得到的产品有焦炭、________。
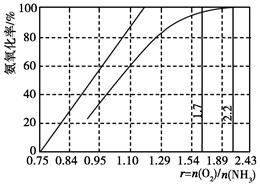
(4 )工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________,实际生产要将r值维持在1.7~2.2之间,原因是________________________________________。
)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨-空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上r[n(O2)/n(NH3)]=________,实际生产要将r值维持在1.7~2.2之间,原因是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个未配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)请将反应物的化学式及配平后的系数填入下列相应的位置中:
| |
| |
查看答案和解析>>
科目:高中化学 来源: 题型:
在智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式是:2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
⑴反应中 元素被氧化, 是氧化剂。
⑵请标出电子转移的方向和数目。 2NaIO3+5NaHSO3=3NaHSO4+2Na2SO4+I2+H2O
⑶反应产物中,氧化产物与还原产物的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应不能发生的是( )
A.CaCO3+2CH3COOH====(CH3COO)2Ca+H2O+CO2↑
B.SiO2+2NaOH====Na2SiO3+H2O
C.AgNO3+HCl====AgCl↓+HNO3
D.2HCl+Cu====CuCl2+ H2↑
H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com