
科目:高中化学 来源:不详 题型:单选题
| A.用分液漏斗分离除去溴苯中混入的溴 |
| B.用盐析法分离硬脂酸钠和甘油 |
| C.蒸馏时,温度计水银球靠近蒸馏烧瓶支管口 |
| D.除去CO2中的少量SO2:通过盛有饱和NaHCO3溶液的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用萃取的方法分离汽油和植物油 |
| B.氯化钠和氯化氢都是电解质,它们在熔融状态下都能导电 |
| C.1LCO一定与1LN2的质量相等 |
| D.失电子越多的物质,其还原性不一定越强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
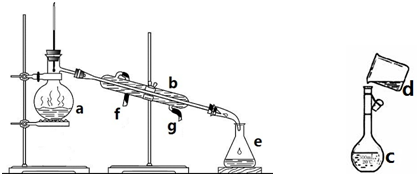
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
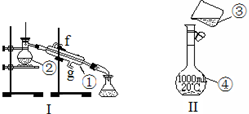
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
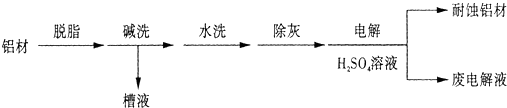
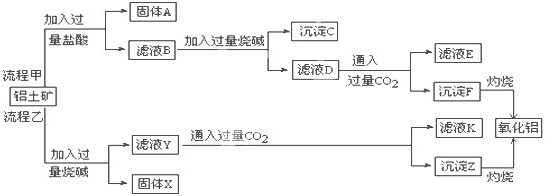
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com