
| A. | 氢氧化钠与盐酸的反应 | B. | H+Cl→HCl | ||
| C. | 氯化铵与氢氧化钡晶体反应 | D. | 金属钠与水反应 |
科目:高中化学 来源: 题型:选择题
| A. | 28g氮气含有的原子数为NA | |
| B. | 4g金属钙的物质的量为1mol | |
| C. | 1mol O2分子的质量等于1mol氧原子的质量 | |
| D. | 24g O2分子和24g O3分子所含的氧原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
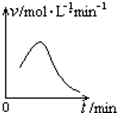 已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示.
已知氯酸钾和亚硫酸氢钠发生氧化还原反应时,生成-1价的氯和+6价的硫的化合物,反应速率v和反应时间t的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
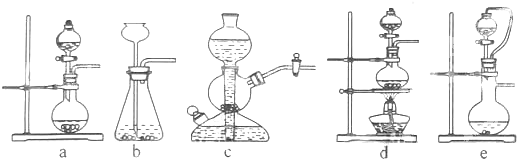
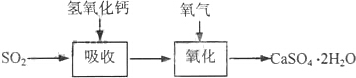
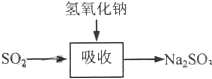
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.9 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3可用于中和胃酸过多 | |
| B. | 硅用于制造光导纤维 | |
| C. | 氯气与澄清石灰水反应制漂白粉 | |
| D. | 医疗上通常直接用无水乙醇进行消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 瓶中气体的黄绿色逐渐变浅,内壁有油状液滴形成 | |
| B. | 若日光直射可能发生爆炸 | |
| C. | 甲烷与氯气发生了取代反应 | |
| D. | 生成物只有 CH3Cl、CH2Cl2、CHCl3、CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
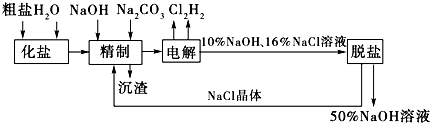
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
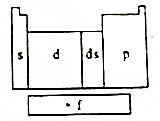 在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示.
在研究原子核外电子排布与元素周期表的关系时,人们发现价电子排布相似的元素集中在一起,据此,人们将元素周期表分为五个区,并以最后填入电子的轨道能级符号作为该区的符号,如图所示.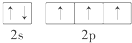 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com