
 如图所示为某有机物的转化关系.完成表格.
如图所示为某有机物的转化关系.完成表格.| 转化序号 | 需加入的反应物及反应条件 |
| ① | |
| ② | |
| ③ | |
| ④ | |
| ⑤ | |
| ⑥ |
分析  中含醇-OH、酚-OH、-COOH,反应①中只有-COOH转化为-COONa,则加试剂为碳酸氢钠可实现转化;反应②中酚-OH、-COOH均发生反应,则加NaOH可实现转化;
中含醇-OH、酚-OH、-COOH,反应①中只有-COOH转化为-COONa,则加试剂为碳酸氢钠可实现转化;反应②中酚-OH、-COOH均发生反应,则加NaOH可实现转化;
反应③为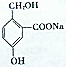 转化为
转化为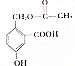 ,-OH与乙酸发生酯化反应,且加硫酸为催化剂,硫酸还可将-COONa转化为-COOH;
,-OH与乙酸发生酯化反应,且加硫酸为催化剂,硫酸还可将-COONa转化为-COOH;
由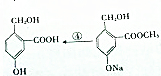 可知,反应④中加硫酸-COOC-转化为-COOH,-ONa转化为酚-OH;
可知,反应④中加硫酸-COOC-转化为-COOH,-ONa转化为酚-OH;
由 $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$ 可知,反应⑤中加NaOH可实现转化;
可知,反应⑤中加NaOH可实现转化;
由 $\stackrel{⑥}{→}$
$\stackrel{⑥}{→}$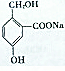 可知,反应⑥中加硫酸发生强酸制取弱酸的反应可实现转化,以此来解答.
可知,反应⑥中加硫酸发生强酸制取弱酸的反应可实现转化,以此来解答.
解答 解: 中含醇-OH、酚-OH、-COOH,反应①中只有-COOH转化为-COONa,则加试剂为碳酸氢钠,发生复分解反应可实现转化;
中含醇-OH、酚-OH、-COOH,反应①中只有-COOH转化为-COONa,则加试剂为碳酸氢钠,发生复分解反应可实现转化;
反应②中酚-OH、-COOH均发生反应,则加试剂为NaOH,发生中和反应可实现转化;
反应③为 转化为
转化为 ,-OH与乙酸发生酯化反应,且加硫酸为催化剂,硫酸还可将-COONa转化为-COOH,即加试剂为浓硫酸、反应条件为加热;
,-OH与乙酸发生酯化反应,且加硫酸为催化剂,硫酸还可将-COONa转化为-COOH,即加试剂为浓硫酸、反应条件为加热;
由 可知,反应④中加硫酸-COOC-转化为-COOH,-ONa转化为酚-OH,则加试剂为稀硫酸;
可知,反应④中加硫酸-COOC-转化为-COOH,-ONa转化为酚-OH,则加试剂为稀硫酸;
由 $\stackrel{⑤}{→}$
$\stackrel{⑤}{→}$ 可知,反应⑤中加试剂为NaOH,-COOC-水解,-COOH、酚-OH与NaOH发生中和反应可实现转化,反应条件为加热;
可知,反应⑤中加试剂为NaOH,-COOC-水解,-COOH、酚-OH与NaOH发生中和反应可实现转化,反应条件为加热;
由 $\stackrel{⑥}{→}$
$\stackrel{⑥}{→}$ 可知,反应⑥中加试剂为硫酸,发生强酸制取弱酸的反应可实现转化,
可知,反应⑥中加试剂为硫酸,发生强酸制取弱酸的反应可实现转化,
故答案为:
| 转化序号 | 需加入的反应物及反应条件 |
| ① | 碳酸氢钠 |
| ② | NaOH |
| ③ | 浓硫酸、加热 |
| ④ | 稀硫酸 |
| ⑤ | NaOH、加热 |
| ⑥ | 硫酸 |
点评 本题考查有机物的合成,为高频考点,把握有机物的官能团与性质、合成反应中官能团的变化为解答的关键,注意酚、羧酸、酯等有机物的性质及相互转化,题目难度不大.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案科目:高中化学 来源: 题型:选择题
 )是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )
)是无色,带有辛辣气味的易燃液体,有毒.人体吸入过多的苯乙烯蒸气时会引起中毒,在空气中的允许浓度在1×10-4 kg•m-3以下.下列关于苯乙烯的性质推断中正确的是( )| A. | 它能使溴的四氯化碳溶液褪色,但不能使酸性高锰酸钾溶液褪色 | |
| B. | 它既能使溴的四氯化碳溶液褪色,也能使酸性高锰酸钾溶液褪色 | |
| C. | 它易溶于水,也易溶于有机溶剂 | |
| D. | 在一定条件下可以发生加聚反应.生成物可用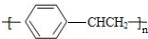 表示 表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3经催化氧化获得NO | B. | NO2跟水作用制取硝酸 | ||
| C. | NH3+CO2+H2O=NH4HCO3 | D. | N2+O2=2NO(放电条件) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA | |
| B. | 12.5mL 16mol•L-1浓硫酸与足量铜反应,转移电子数为0.2NA | |
| C. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| D. | 1 mol的甲基与1 mol的铵根离子所含电子数均为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | T、W、M的最高价氧化物的水化物相互反应 | |
| B. | T、Y、W组成的化合物溶于含酚酞的水,溶液显红色 | |
| C. | 简单离子半径:r(W)>r(M)>r(Y)>r(X) | |
| D. | 简单氢化物的稳定性:X>T>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | HOOC-COOH | C. | HOCH2CH2OH | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 金刚烷(C10H16)的结果如图所示,它可以看成四个等同的六元环组成的空间构型.该金刚烷的二氯代物的数目是( )
金刚烷(C10H16)的结果如图所示,它可以看成四个等同的六元环组成的空间构型.该金刚烷的二氯代物的数目是( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
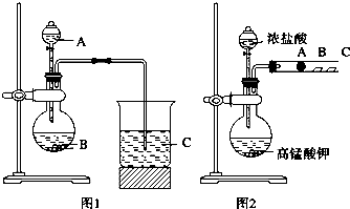
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-═ClO-+Cl?+H2O | |
| B. | 该消毒液的pH约为12:ClO-+H2O?HClO+OH-? | |
| C. | 该消毒液与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:2H++Cl-+ClO-═Cl2↑+H2O | |
| D. | 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ClO-═HClO+CH3COO-? |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com