
【题目】化学与生活,社会发展息息相关,下列有关说法不正确的是( )
A. 14C可用于文物年代的鉴定,12C和14C互为同位素
B. 甲烷的燃烧热很高,是较清洁的燃料,但它是温室气体
C. 在元素周期表中所含元素种类最多的族是IIIB族
D. 碱金属元素自上而下金属性逐渐增强,熔沸点依次升高
科目:高中化学 来源: 题型:
【题目】以石油裂解产物烯烃为原料合成一些新物质的路线如下. 
已知: ![]() +
+![]()
![]()
![]()
完成下列填空:
(1)B与乙烯发生反应的类型是 , 甲的结构简式为 .
(2)写出A→B的化学方程式 .
(3)写出符合下列条件的W的一种同分异构体的结构简式 .
①遇FeCl3溶液显紫色,但不能与浓溴水反应;
②1H﹣NMR谱显示有四种不同化学环境的氢原子.
(4)下列说法不正确的是(填选项字母).
A.化合物A,C均能使酸性KMnO4溶液褪色
B.1molW生成1molR仅需要2mol的H2
C.化合物Y属于酯类的同分异构体有4种
D.化合物R分子式为C9H18O2
(5)写出上图中B到C的合成路线(无机试剂任选) . (合成路线常用的表示方式为:A ![]() B
B ![]() …目标产物)
…目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(g)+3Y(g)2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),平衡时X、Y、Z的浓度分别为0.1molL﹣1、0.3molL﹣1、0.08molL﹣1 , 则下列判断正确的是( )
A.c1:c2的值不能确定
B.平衡时,Y和Z的生成速率之比为1:1
C.0.48molL﹣1<c1+c2+c3<0.56molL﹣1
D.c1的取值范围为0<c1<0.14 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将100mL某硝酸和硫酸的混合液分成两等份:一份加入过量的BaCl2溶液,充分反应后得沉淀2.33g;另一份加入50mL1.0molL﹣1NaOH溶液,充分反应后溶液的pH=13(溶液的体积为100mL).试计算:
(1)原溶液中所含H2SO4的物质的量mol.
(2)原混合溶液中硝酸的物质的量浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜常用作有机合成工业中的催化剂,为白色晶体,不溶于乙醇,微溶于水,易溶于浓盐酸形成络合离子[CuCl2]﹣ . 受潮露置空气中迅速氧化成碱式盐.实验室用下列流程制备: 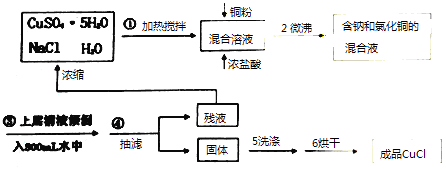
注:①实验药品:硫酸铜晶体12.5g、氯化钠晶体6.0g、水200mL、铜粉3.5g、浓盐酸10mL.
②Na[CuCl2](易电离,溶液无色) ![]() NaCl+CuCl↓ (白色沉淀).
NaCl+CuCl↓ (白色沉淀).
请回答:
(1)写出实验室制取Na[CuCl2]的离子方程式 .
(2)判断步骤②反应完全的现象是 .
(3)步骤④有关抽滤操作,下列说法正确的是 .
A.选择抽滤主要是为了加快过滤速度,得到较干燥的沉淀
B.在吸滤瓶和抽气泵之间应连接一个安全瓶,吸滤瓶应与安全瓶的长导管相接
C.抽滤时不宜过滤胶状沉淀,否则易在滤纸上形成一层密实的沉淀
D.洗涤沉淀时,应关小水龙头,使洗涤剂缓缓通过沉淀物
(4)步骤⑤用乙醇的水溶液洗涤的目的是 .
(5)步骤⑥烘干须在真空干燥箱中进行,其原因是 .
(6)氯化亚铜的定量分析:
①取样品0.25g和10mL过量的FeCl3溶液于250mL锥形瓶中,充分溶解.
②用0.10molL﹣1硫酸锶铈标准溶液滴定.
已知:CuCl+FeCl3=CuCl2+FeCl2; Fe2++Ce4+=Fe3++Ce3+三次平行试验结果如下(平行试验结果相差不能超过1%):
平行试验次数 | 1 | 2 | 3 |
0.25g样品消耗硫酸铈标准溶液的体积(mL) | 24.35 | 24.05 | 23.95 |
则样品中CuCl的纯度为 . (结果保留三位有效数字)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于某可逆反应的下列叙述中,不能说明反应一定达到平衡的是( )
A. 正反应速率与逆反应速率相等
B. 反应物的浓度与生成物的浓度不再改变
C. 在给定条件下反应达到最大限度
D. 反应物的浓度与生成物的浓度相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:请回答下列问题:
3Zn+2K2FeO4+8H2O ![]() 3Zn(OH)2+2Fe(OH)3+4KOH.
3Zn(OH)2+2Fe(OH)3+4KOH.
(1)高铁电池的负极材料是 .
(2)放电时,正极发生(填“氧化”或“还原”)反应;已知负极反应为Zn﹣2e﹣+2OH﹣═Zn(OH)2 , 则正极反应为 .
(3)放电时,(填“正”或“负”)极附近溶液的碱性增强.
(4)充电时,阴极的电极反应式为 .
(5)充电时,理论上分析,每生成0.15moLK2FeO4转移电子数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有较大量的Cl-、CO32-、OH-3种阴离子,如果只取一次该溶液就能分别将3种阴离子依次检验出来,下列实验操作顺序(滴加的试剂均过量)正确的是( )
①滴加Mg(NO3)2溶液; ②过滤; ③滴加AgNO3溶液; ④滴加Ba(NO3)2溶液
A.①②④②③B.①②③②④C.④②①②③D.④②③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com