
重铬酸钾又名红矾钾,是化学实验室中的一种重要分析试剂。工业上以铬酸钾(K2CrO4)为原料,采用电化学法制备重铬酸钾(K2Cr2O7)。制备装置如下图所示(阳离子交换膜只允许阳离子透过):
制备原理:2CrO42-(黄色)+2H+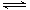 Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)通电后阳极室产生的现象为 ,其电极反应式是 。
(2)该制备过程总反应的离子方程式可表示为4CrO42-+4H2O="2" Cr2O72- + 4OH- +2H2↑+O2↑,若实验开始时在右室中加入38.8g K2CrO4,t分钟后测得右室中K与Cr的物质的量之比为3:2,则溶液中K2CrO4和K2Cr2O7的物质的量之比为 ;此时电路中转移电子的物质的量为 。
(每空2分,共8分)
(1)阳极产生无色气体,溶液由黄色逐渐变为橙色;
4OH--4e-=O2↑+2H2O 或2H2O-4e-=O2↑+4H+
(2)2:1 ; 0.1 mol
解析试题分析:(1)电解池中阳极失去电子,发生氧化反应。则阳极是溶液中的OH-放电生成氧气,电极反应式是4OH--4e-=O2↑+2H2O。由于OH-被电解,破坏了阳极周围水的电离平衡导致阳极周围溶液显酸性,则促进可逆反应向2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O正反应方向移动,所以阳极周围的实验现象是阳极产生无色气体,溶液由黄色逐渐变为橙色。
Cr2O72-(橙色)+H2O正反应方向移动,所以阳极周围的实验现象是阳极产生无色气体,溶液由黄色逐渐变为橙色。
(2)设溶液中K2CrO4和K2Cr2O7的物质的量分别是x和y,则(2x+2y):(x+2y)=3:2,解得x:y=2:1。38.8g K2CrO4的物质的量是38.8g÷194g/mol=0.2mol,所以根据Cr原子守恒可知,生成的K2Cr2O7的物质的量是0.05mol。根据方程式4CrO42-+4H2O=2 Cr2O72- + 4OH- +2H2↑+O2↑,每生成2molK2Cr2O7,反应中转移4mol电子,所以此时电路中转移电子的物质的量为0.05mol×4=0.1mol。
考点:考查电解原理的有关应用、判断和计算


科目:高中化学 来源: 题型:填空题
近年来,为提高能源利用率,西方提出共生理念——为提高经济效益,人类生产活动尽可能多功能化.共生工程将会大大促进化学工业的发展.
(1)由于共生工程的应用,利用发电厂产生的SO2制成自发电池,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06V.实际过程中,将SO2通入电池的 极(填“正”或“负”),负极反应式为 .用这种方法处理SO2废气的优点是 .
(2)以硫酸工业的SO2尾气、氨水、石灰石、焦炭、碳酸氢铵和氯化钾等为原料,可以合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质.合成路线如下:
①生产中,向反应Ⅱ中的溶液中加入适量还原性很强的对苯二酚等物质,其目的是 .
②下列有关说法正确的是 .
| A.反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙 |
B.反应Ⅲ中发生反应的化学方程式为CaSO4+4C CaS+4CO↑ CaS+4CO↑ |
| C.反应Ⅳ需控制在60~70℃,目的之一是减少碳酸氢铵的分解 |
| D.反应Ⅴ中的副产物氯化铵可用作氮肥 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(15分)氯化亚铜(CuCl)是一种白色固体,微溶于水,不溶于酒精。研究该物质的应用新领域、生产新方法及生产过程中的环保新措施都具有重要意义。
(1)镁—氯化亚铜海水电池,可用于鱼雷上。该电池被海水激活时,正极导电能力增强,同时产生气泡,则正极上被还原的物质有 、 (填化学式)。
(2)工业上以铜作催化剂,氯代甲烷和硅粉反应合成甲基氯硅烷的过程中产生大量废渣(主要成分为硅粉、铜、碳等)。某课外小组以该废渣为原料制CuCl,流程示意图如下: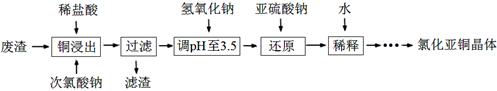
回答下列问题:
①氯代甲烷有4种,其中属于重要工业溶剂的是 (写出化学式)。
②“还原”阶段,SO32-将Cu2+还原得[CuCl2]-,完成下列离子方程式。 Cu2++
Cu2++ Cl-+
Cl-+ SO32-+
SO32-+ =
= [CuCl2]-+
[CuCl2]-+ +
+
③在稀释过程中存在下列两个平衡:
ⅰ [CuCl2]- CuCl+Cl- K=2.32
CuCl+Cl- K=2.32
ⅱ CuCl(s) Cu+(aq)+Cl- Ksp=1.2×10-6
Cu+(aq)+Cl- Ksp=1.2×10-6
当[CuCl2]-完成转化时(c([CuCl2]-)≤1.0×10-5 mol·L-1),溶液中c(Cu+)≥ 。
④获得CuCl晶体需经过滤、洗涤、干燥。洗涤时,常用无水乙醇代替蒸馏水做洗涤剂的优点是 (写一点)。
(3)工业生产CuCl过程中产生浓度为2~3 g·L-1的含铜废水,对人及环境都有较大的危害,必须进行回收利用。用萃取法富集废水中的铜,过程如下:
①实验室完成步骤ⅰ时,依次在分液漏斗中加入曝气后的废水和有机萃取剂,经振荡并 后,置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先 ,然后打开活塞放出下层液体,上层液体从上口倒出。
②写出步骤ⅱ的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
向8 g某二价金属的氧化物固体中加入稀硫酸,使其恰好完全溶解,已知消耗硫酸的体积为100 mL,在所得溶液中插入铂电极进行电解,通电一定时间后,在一个电极上收集到224 mL(标准状况)氧气,在另一个电极上析出该金属1.28 g。
(1)根据计算确定金属氧化物的名称。
(2)求通电后硫酸溶液的物质的量浓度(溶液体积按100 mL计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
(18分)废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法回收WC和制备CoxOy,的工艺流程简图如下:

(1)电解时废旧刀具作阳极,不锈钢作阴极,盐酸的作用是______。
(2)通人氨气的目的是调节溶液的pH,除去铁元素。由表中的数据可知,理论上可选择pH最大范围是____________。
(3)实验测得NH4HCO3溶液显碱性,制备CoCO3时,选用的加料方式是_______(填代号),原因是_______。
a.将滤液与NH4HCO3溶液同时加入到反应容器中
b.将滤液缓慢加入到盛有NH4HCO3溶液的反应容器中
c.将NH4HCO3溶液缓慢加入到盛有滤液的反应容器中
写出生成CoCO3的离子方程式______________________________________。
(4)实验中获得的若洗涤不充分,在焙烧时会产生污染性气体,该污染性气体的成分为_______________(填化学式)。
(5)实验室用下列装置制取 ,并测定其化学式。
,并测定其化学式。
①装置A制得的中含有少量Cl2,则装置B中所盛放的试剂为______(填代号)。
a.NaHCO3溶液 b.NaOH溶液 c.KMnO4溶液 d.饱和NaCI溶液
②在CoCO3完全转化为 后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物
后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物 的化学式为____________。
的化学式为____________。
③若缺少装置F,则导致 的值______(填“偏大”、“偏小”或“无影响”)。
的值______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
某小组按图1所示的装置探究铁的吸氧腐蚀。完成下列填空:

(1)图2 是图1所示装置的示意图,在图2的小括号内填写正极材料的化学式;在方括号内用箭头表示出电子流动的方向。
(2)写出正、负极反应的方程式。正极: ,负极: 。
(3)按图1装置实验,约8分钟才看到的导管中液柱上升,下列措施可以更快更清晰地观察到液柱上升的是 。
a.用纯氧气代替具支试管内的空气
b.用食盐水浸泡过的铁钉再蘸取铁粉和炭粉的混合物
c.用毛细尖嘴管代替玻璃导管,并向试管的水中滴加少量红墨水
(4)升高温度可以加快化学反应速率,建议用酒精灯加热具支试管。这一措施 (填“可行”或“不行”)。
(5)有同学观察到图1装置在组装时就会使导管中液面低于试管中液面,导致实验时导管中液柱上升需要更多的时间。图1装置组装时,使导管中液面低于试管中液面的原因是 。消除这一现象的简单操作是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是
①可能有C2H2
②一定有CH4
③一定有C3H8
④一定没有C2H6
⑤可能有C2H6
| A.②⑤ | B.②④ | C.③④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某含碳?氢?氧的有机物A能发生如图所示的变化:已知A?C?D?E均能在一定条件下与新制的氢氧化铜悬浊液反应生成红色沉淀,则A的同分异构体是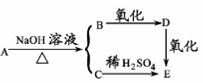
| A.乙酸 | B.甲酸乙酯 | C.甲酸甲酯 | D.乙酸甲酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
两种气态烃组成的混合气体,完全燃烧后得到CO2和H2O的物质的量随着混合烃物质的量的变化如图所示,则下列对混合烃的判断正确的是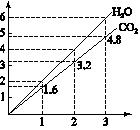
①可能有C2H4 ②一定有CH4 ③一定有C3H8
④一定没有C2H6 ⑤可能有C2H6 ⑥可能有C2H2
| A.②⑤⑥ | B.①②④ | C.④⑥ | D.②③ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com