
| A.等质量的硫蒸气和硫磺分别完全燃烧,后者放出的热量多 |
B.氢气的燃烧热为285.8kJ ·  ,则氢气燃烧的热化学方程式为 ,则氢气燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ·  |
| C.Ba(OH)2 · 8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l);△H<0 |
| D.某酸溶液可以与石灰石反应放出CO2,则该酸不一定为强酸。 |
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol可燃物燃烧生成氧化物放出的热量就是该物质的燃烧热 |
| B.因为醋酸是弱电解质,盐酸是强电解质,所以中和等体积等物质的量浓度的醋酸和盐酸时,中和醋酸消耗的NaOH比盐酸消耗的NaOH用量少 |
| C.反应物总能量大于生成物总能量的反应是放热反应 |
| D.强电解质溶液的导电能力比弱电解质溶液的导电能力强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2(t-BuNO),测得该反应的ΔH =" +50.5" kJ·mol-1,活化能Ea =" 90.4" kJ·mol-1。能量关系图合理的是
2(t-BuNO),测得该反应的ΔH =" +50.5" kJ·mol-1,活化能Ea =" 90.4" kJ·mol-1。能量关系图合理的是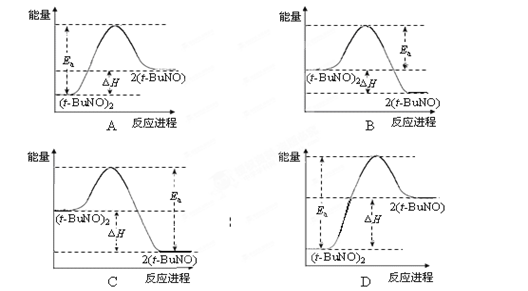
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.化学反应除了生成新物质外,还伴随着能量的变化 |
| B.放热反应都不需要加热就可以发生 |
| C.需要加热的化学反应都是吸热反应 |
| D.化学反应放热还是吸热,取决于反应条件 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.二氧化碳与超临界水作用生成汽油的反应属于放热反应? |
| B.“水热反应”是一种复杂的物理化学变化 |
| C.火力发电厂可以利用废热,将二氧化碳转变为能源物质 |
| D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1mol N2(g)和1mol O2(g)反应放出的能量为180kJ |
| B.1mol N2(g)和1mol O2(g)具有的总能量小于2mol NO(g)具有的总能量 |
| C.通常情况下,N2(g)和O2(g)混合能直接生成NO |
| D.NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N键吸收941kJ热量,则( )
N键吸收941kJ热量,则( )
| A.N4与N2互称为同位素 |
| B.1molN4气体转化为N2时要吸收748kJ能量 |
| C.N4是N2的同系物 |
| D.1molN4气体转化为N2时要放出724kJ能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com