
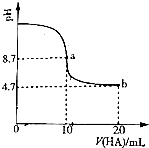
·ÖĪö £Ø1£©ŅŗĆęÉĻÓŠ“óĮæ°×Īķ£¬µČ°×ĪķĻūŹ§ŗó£¬ĶłČÜŅŗÖŠµĪ¼ÓAgNO3ČÜŅŗ£¬ÓŠ²»ČÜÓŚĻ”HNO3µÄÄżČéד°×É«³Įµķ²śÉś£¬ĖµĆ÷°×ĪķĪŖŃĪĖįµÄŠ”ŅŗµĪ£¬¼“»į²śÉśHCl£»Ķ¬Ź±ÓŠ“ų“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢåŅŻ³ö£¬øĆĘųĢåæÉŹ¹µĪÓŠĘ·ŗģŹŌŅŗµÄĀĖÖ½ĶŹÉ«ĖµĆ÷ŹĒSO2£»
£Ø2£©ÓĆSOCl2ÓėFeCl3•6H2O»ģŗĻ¹²ČČ£¬æɵĆĪŽĖ®FeCl3£¬ŹĒŅņSOCl2ÓėĖ®·“Ó¦¼Č¼õÉŁæÉĖ®µÄĮæ£¬Éś³ÉµÄHClÓÖŅÖÖĘĮĖFeCl3µÄĖ®½ā£®
½ā“š ½ā£ŗ£Ø1£©SOCl2ŹĒŅ»ÖÖŅŗĢ¬»ÆŗĻĪļ£¬ÓėĖ®·¢Éś¾ēĮŅµÄ·ĒŃõ»Æ»¹Ō·“Ó¦£¬Éś³ÉĮ½ÖÖÓŠ“Ģ¼¤ŠŌĘųĪ¶µÄĘųĢ壬øĆĮ½ÖÖĘųĢåÓ¦øĆĪŖĀČ»ÆĒāŗĶ¶žŃõ»ÆĮņ£¬·“Ó¦µÄ·½³ĢŹ½ĪŖSOCl2+H2O=2HCl”ü+SO2”ü£¬¹Ź“š°øĪŖ£ŗSOCl2+H2O=2HCl”ü+SO2”ü£»
£Ø2£©½«FeCl3ČÜŅŗÖ±½ÓÕōøÉµĆ²»µ½ĪŽĖ®FeCl3£¬ŌŅņŹĒĀČ»ÆĢśĖ®½ā³öµÄHClŹĒ»Ó·¢ŠŌĖį£¬HClµÄ»Ó·¢µ¼ÖĀĀČ»ÆĢśµÄĖ®½ā±»“Ł½ų£¬¹ŹÕōøÉŗóµĆFe£ØOH£©3£»SOCl2ÓėĖ®·“Ӧɜ³ÉµÄĀČ»ÆĒā»į¶ŌĀČ»ÆĢśĖ®½āĘšµ½ŅÖÖĘ×÷ÓĆ£»·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗSOCl2+H2O=2HCl”ü+SO2”ü£¬ÕōøÉFeCl3ČÜŅŗ²»ÄܵƵ½ĪŽĖ®FeCl3£¬Ź¹SOCl2ÓėFeCl3•6H20»ģŗĻ²¢¼ÓČČ£¬æɵƵ½ĪŽĖ®FeCl3£¬SOCl2ÓėĖ®·“Ӧɜ³ÉµÄĀČ»ÆĒā»į¶ŌĀČ»ÆĢśĖ®½āĘšµ½ŅÖÖĘ×÷ÓĆ£¬
¹Ź“š°øĪŖ£ŗFe£ØOH£©3£»SOCl2ĻūŗÄFeCl3•6H2O ÖŠµÄ½į¾§Ė®£¬²¢²śÉśHCl£¬ŅÖÖĘFeCl3µÄĖ®½ā£®
µćĘĄ ±¾Ģāæ¼²éĮĖŌŖĖŲ»ÆŗĻĪļµÄŠŌÖŹ£¬ĪŖøßĘµæ¼µć£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦µÄ漲飬ÄŃ¶Č²»“ó£¬ÄÜÕżČ·ÅŠ¶ĻSOCl2ŗĶĖ®·“Ó¦µÄÉś³ÉĪļŹĒ½ā±¾ĢāµÄ¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ×īĶā²ćµē×ÓŹż£ŗZ£¾R£¾Y | |
| B£® | ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗY£¼Z | |
| C£® | R”¢XµÄŃõ»ÆĪļ¾łĪŖĄė×Ó»ÆŗĻĪļ | |
| D£® | XŗĶYĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļÄÜĻą»„·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | “ĪĀČĖįµÄ½į¹¹Ź½£ŗH-Cl-O | B£® | ĀĮĄė×Ó½į¹¹Ź¾ŅāĶ¼£ŗ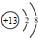 | ||
| C£® | ¼×Ķé·Ö×ÓµÄĒņ¹÷Ä£ŠĶ£ŗ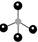 | D£® | Č©»łµÄµē×ÓŹ½£ŗ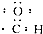 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šŹōÄĘ“ę·ÅŌŚŹŌ¼ĮĘæÖŠµÄĆŗÓĶĄļ | |
| B£® | “ę·ÅŅŗäåµÄŹŌ¼ĮĘæÖŠÓ¦¼ÓĖ®·ā | |
| C£® | ĻõĖįÓ¦ÓĆ×ŲÉ«ĘæŹ¢×°ĒŅ±Ü¹ā“ę·Å | |
| D£® | ÉÕ¼īÓ¦Ź¢·ÅŌŚ²£Į§ČūµÄÄ„æŚ²£Į§ĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
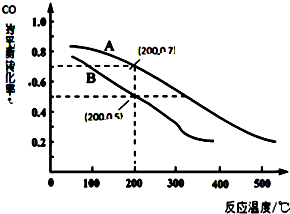 æĘѧ¼ŅæŖ·¢³öŅ»ÖÖ”°½ą¾»Ćŗ¼¼Źõ”±£¬ĶعżĻņµŲĻĀĆŗ²ć”°Ęų»ÆĀÆ”±ÖŠ½»Ģę¹ÄČėæÕĘųŗĶĖ®ÕōĘųµÄ·½·Ø£¬Į¬Šų²ś³öøßČČÖµµÄĆŗĢæĘų£¬ĘäÖ÷ŅŖ³É·ÖŹĒCOŗĶH2£®”°Ęų»ÆĀÆ”±ÖŠÖ÷ŅŖ·“Ó¦ÓŠ£ŗ
æĘѧ¼ŅæŖ·¢³öŅ»ÖÖ”°½ą¾»Ćŗ¼¼Źõ”±£¬ĶعżĻņµŲĻĀĆŗ²ć”°Ęų»ÆĀÆ”±ÖŠ½»Ģę¹ÄČėæÕĘųŗĶĖ®ÕōĘųµÄ·½·Ø£¬Į¬Šų²ś³öøßČČÖµµÄĆŗĢæĘų£¬ĘäÖ÷ŅŖ³É·ÖŹĒCOŗĶH2£®”°Ęų»ÆĀÆ”±ÖŠÖ÷ŅŖ·“Ó¦ÓŠ£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ĶØæÕĘųŹ±£¬Ķ±»øÆŹ“£¬±ķĆę²śÉśCuO | |
| B£® | ·ÅµēŹ±£¬Li+Ķø¹ż¹ĢĢåµē½āÖŹĻņCu¼«ŅĘ¶Æ | |
| C£® | ·ÅµēŹ±£¬Õż¼«µÄµē¼«·“Ó¦Ź½ĪŖCu2O+H2O+2e-ØT2Cu+2OH- | |
| D£® | Õūøö·“Ó¦¹ż³ĢÖŠ£¬ĶĻąµ±ÓŚ“߻ƼĮ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1000 mL£¬514.00 g | B£® | 480 mL£¬198.72 g | ||
| C£® | 500 mL£¬207.00 g | D£® | ČĪŅā¹ęøń£¬207.00 g |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ壬ĘäŌĄķŹĒ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4KJ/mol£¬
ŗĻ³É°±¹¤Ņµ¶Ō¹śĆń¾¼ĆŗĶÉē»į·¢Õ¹¾ßÓŠÖŲŅŖµÄŅāŅ壬ĘäŌĄķŹĒ£ŗN2£Øg£©+3H2£Øg£©?2NH3£Øg£©”÷H=-92.4KJ/mol£¬| ²»Ķ¬Ź±¼äø÷ĪļÖŹµÄĪļÖŹµÄĮæ/mol | |||||
| 0min | 1min | 2min | 3min | 4min | |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·Šµć/”ę | |
| SiHCl3 | 33.0 |
| SiCl4 | 57.6 |
| HCl | -84 |
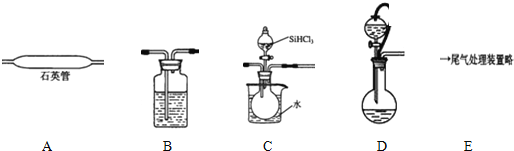
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com