
 铜是过渡金属元素,可以形成多种化合物.
铜是过渡金属元素,可以形成多种化合物.
分析 (1)Cu是29号元素,原子核外电子数为29,根据核外电子排布规律书写核外电子排布式;
(2)Cu+有2个空的sp杂化轨道,NH3分子中的N原子有一孤电子对,进入Cu+空的sp杂化轨道,以配位键形成直线形结构;
(3)①根据N原子形成的共价键判断;
②同周期自左而右,电负性增大,据此判断C、N元素的电负性;
③乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,但三甲胺[N(CH3)3]分子之间不能形成氢键;
④由图可知:离子中存在配位键、C-N键、C-H键、N-H键、C-C键,据此判断离子化学键类型;
(4)利用均摊法确定M的化学式,铜离子和二氧化硫能发生氧化还原反应生成亚铜离子和硫酸根离子.
解答 解:(1)Cu是29号元素,原子核外电子数为29,基态原子核外电子排布式为1s22s22p63s23p63d104s1,故答案为:1s22s22p63s23p63d104s1;
(2)Cu+有2个空的sp杂化轨道,NH3分子中的N原子有一孤电子对,进入Cu+空的sp杂化轨道,以配位键形成直线形结构,则[Cu(NH3)n]+中Cu+与2个氮原子形成配位键,
故答案为:直线形;2;
(3)①乙二胺分子中氮原子形成4个共价键,则价层电子对数为4,其轨道的杂化类型为sp3杂化,故答案为:sp3杂化;
②同周期自左而右,电负性增大,电负性N>C,故答案为:N>C;
③乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高,
故答案为:乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键;
③[Cu(en)2]Cl2中存在配位键、离子键、C-N键、C-H键、N-H键、C-C键,其中C-N键、C-H键、N-H键为极性键,C-C键为非极性键,故不存在氢键和金属键;
故答案为:E、F;
(4)根据晶胞结构知,白色小球个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,黑色小球个数=4,所以该化合物的化学式为:CuCl,二氧化硫有还原性,铜离子有氧化性,所以二氧化硫和氯化铜发生氧化还原反应生成氯化亚铜和硫酸,离子反应方程式为:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+SO42-+4H+,
故答案为:2Cu2++2Cl-+SO2+2H2O=2CuCl↓+SO42-+4H+.
点评 本题考查核外电子排布规律、电负性、杂化轨道、分子空间结构、氢键与化学键、配位键等,综合性较大,难度中等,是对知识的综合运用,需要学生具备扎实的基础与分析问题解决问题的能力.


科目:高中化学 来源: 题型:选择题
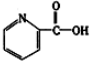 ②阿斯匹林
②阿斯匹林
 ④东茛菪内酯
④东茛菪内酯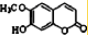
| A. | ①④ | B. | ②④ | C. | ①③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 核外电子排布相同的微粒,其化学性质也相同 | |
| B. | 含有金属元素和非金属元素的化合物不一定是离子化合物 | |
| C. | 仅含非金属元素的化合物一定是共价化合物 | |
| D. | 凡需要加热的反应一定是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
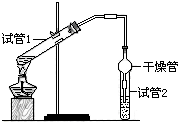 乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.为证明浓硫酸在实
乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.为证明浓硫酸在实| 实验 编号 | 试管1中的试剂 | 试管2中试剂 | 测得有机层的厚度/cm |
| A | 2mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 饱和碳酸钠溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
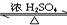 CH3CO18OC2H5+H2O.
CH3CO18OC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
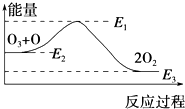 氯原子对O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.
氯原子对O3的分解有催化作用:O3+Cl═ClO+O2△H1,ClO+O═Cl+O2△H2.| A. | 反应O3+O═2O2的△H=E1-E3 | B. | 反应O3+O═2O2是吸热反应 | ||
| C. | △H=△H1+△H2 | D. | 氯原子没有改变O3分解反应的历程 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
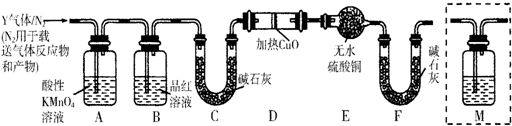
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| W | Z | ||
| T |
| A. | X、Y、Z的原子半径r(T)>r(W)>r(Z) | |
| B. | 由X、Y、Z氢化物的热稳定性X>Y>Z | |
| C. | X最高价氧化物对应的水化物的酸性比W的弱 | |
| D. | W元素的单质具有半导体的特性,可以用于制造光导纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
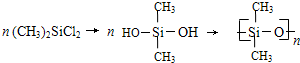 ,其合成过程中涉及的反应类型分别是( )
,其合成过程中涉及的反应类型分别是( )| A. | ①③ | B. | ①② | C. | ②④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com