


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:不详 题型:单选题
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.密度:CH3CH2CH2Cl>CH3CH2Cl>CH3Cl | B.水溶性: HCl>H2S> SO2 |
| C.还原性:HF>HCl>HBr>HI | D.热稳定性:HF>H2O>NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
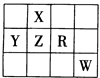
| A.五种元素可能都是金属元素 |
| B.五种元素的原子最外层电子数一定都大于2 |
| C.X的氢化物的沸点一定比Z的氢化物的沸点高 |
| D.R的最高价氧化物对应的水化物一定是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在短周期元素中X的金属性最强 |
| B.Y的最高价含氧酸属于弱酸 |
| C.原子半径Z>Y,离子半径Z2-> X+ |
| D.Y、Z都可与氢元素形成氢化物,Z的氢化物比Y的氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第二周期第ⅣA族 | B.第三周期第ⅣA族 |
| C.第三周期第ⅥA族 | D.第二周期第ⅥA族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com