
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CO、 2mol H2 | 1mol CH3OH | 2mol CO、 4mol H2 |
| CH3OH的浓度/mol•L-1 | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 反应物转化率 | α1 | α2 | α3 |

分析 (1)对于可逆反应,升高温度,正逆反应速率均加快,$\frac{n[Ni(CO)_{4}]}{{n}^{4}(CO)}$=K(平衡常数),因此温度不变,比值不变,反应达到平衡后,充入CO再次达到平衡时,相当于增大压强,平衡右移,CO的体积分数降低,Ni与CO反应,随反应的进行,气体质量增大,直到反应达到平衡,质量才不发生变化,根据公式ρ=m/V,容器容积V不变,密度ρ不变时,说明质量m不再变化,反应达到化学平衡状态;
(2)根据上述反应,在50~80℃,Ni与CO化合生成Ni(CO)4,在180~200℃分解生成Ni和CO,因此T1<T2,反应中CO可循环利用;
(3)根据反应特点可以确定,甲和乙可建立相同平衡状态,因此平衡时:c1=c2,Q1+Q2=90.8,α1+α2=100%.比较甲和丙,开始时丙中CO和H2浓度均为甲的2倍,相对于甲,丙相当于加压.假设甲和丙建立相同的平衡状态,则丙中放热是甲中的2倍,但加压平衡右移,因此Q3>2Q1,α3>α1,因此α2+α3>100%;
(4)反应中含有CO,CO会还原Cu2O,加入少量CO2,可使CO还原Cu2O反应逆向移动,保持Cu2O的量不变,反应为Cu2O+CO?2Cu+CO2;
(5)甲醇不完全燃烧生成一氧化碳和水蒸气的反应为CH3OH+O2═CO+2H2O.根据盖斯定律计算;
(6)用CO还原金属氧化物,反应的平衡常数K均可表示为$[\frac{c(C{O}_{2})}{c(CO)}]^{n}$,n>0,因此lg$\frac{c(C{O}_{2})}{c(CO)}$越小,则平衡常数越大.对于CO还原Cr2O3和SnO2,温度升高lg$\frac{c(C{O}_{2})}{c(CO)}$减小,则平衡常数增大,平衡正向移动,因此这两个反应为吸热反应,对于CO还原PbO2和Cu2O的反应为放热反应.
解答 解:(1)对于可逆反应,升高温度,正逆反应速率均加快,A错误.$\frac{n[Ni(CO)_{4}]}{{n}^{4}(CO)}$=K(平衡常数),因此温度不变,比值不变,B错误.反应达到平衡后,充入CO再次达到平衡时,相当于增大压强,平衡右移,CO的体积分数降低,C正确.Ni与CO反应,随反应的进行,气体质量增大,直到反应达到平衡,质量才不发生变化,根据公式ρ=m/V,容器容积V不变,密度ρ不变时,说明质量m不再变化,反应达到化学平衡状态,D正确;
故选CD;
(2)根据上述反应,在50~80℃,Ni与CO化合生成Ni(CO)4,在180~200℃分解生成Ni和CO,因此T1<T2,反应中CO可循环利用;
故答案为:<;CO;
(3)根据反应特点可以确定,甲和乙可建立相同平衡状态,因此平衡时:c1=c2,a正确;Q1+Q2=90.8,c正确;α1+α2=100%.比较甲和丙,开始时丙中CO和H2浓度均为甲的2倍,相对于甲,丙相当于加压.假设甲和丙建立相同的平衡状态,则丙中放热是甲中的2倍,但加压平衡右移,因此Q3>2Q1,b错误;α3>α1,因此α2+α3>100%,d错误;
故答案为:ac;
(4)反应中含有CO,CO会还原Cu2O,加入少量CO2,可使CO还原Cu2O反应逆向移动,保持Cu2O的量不变,反应为Cu2O+CO?2Cu+CO2;
故答案为:Cu2O+CO?2Cu+CO2;
(5)甲醇不完全燃烧生成一氧化碳和水蒸气的反应为CH3OH+O2═CO+2H2O.根据盖斯定律,反应CH3OH(l)+O2(g)═CO(g)+2H2O(g)的△H=-725.8 kJ•mol-1-
(-283 kJ•mol-1)-2×(-44.0 kJ•mol-1)=-354.8 kJ•mol-1;
故答案为:CH3OH(l)+O2(g)═CO(g)+2H2O(g)△H=-354.8 kJ•mol-1;
(6)用CO还原金属氧化物,反应的平衡常数K均可表示为$[\frac{c(C{O}_{2})}{c(CO)}]^{n}$,n>0,因此lg$\frac{c(C{O}_{2})}{c(CO)}$越小,则平衡常数越大.对于CO还原Cr2O3和SnO2,温度升高lg$\frac{c(C{O}_{2})}{c(CO)}$减小,则平衡常数增大,平衡正向移动,因此这两个反应为吸热反应,对于CO还原PbO2和Cu2O的反应为放热反应;一氧化碳还原Cr2O3的反应为3CO(g)+Cr2O3(s)?2Cr(s)+3CO2(g),在700℃用一氧化碳还原Cr2O3时,lg$\frac{c(C{O}_{2})}{c(CO)}$=4,$\frac{c(C{O}_{2})}{c(CO)}$=10-4,K=(10-4)3=10-12;
故答案为:Cr2O3、SnO2;10-12.
点评 本题考查较为综合,涉及化学平衡影响因素的分析判断,反应速率的计算应用,为高频考点,侧重于学生的分析能力和计算能力的考查,平衡移动原理的应用是解题关键,依据反应特征设计制备过程是解题关键,题目难度较大.


科目:高中化学 来源: 题型:解答题
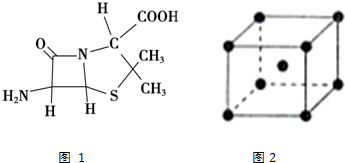
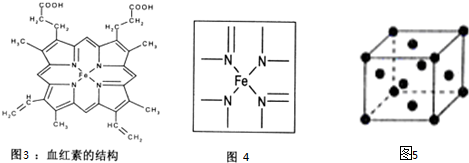
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 往蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,再水浴加热,能看到银镜生成 | |
| C. | 淀粉和纤维素的分子式均为(C6H10O5)n,二者互为同分异构体 | |
| D. | 向鸡蛋清溶液中加硫酸铵饱和溶液,有沉淀析出,再加水沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
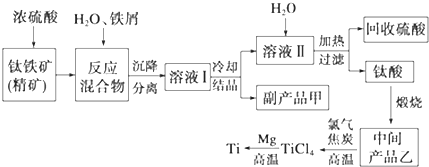
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ① | ② | ③ | ④ | |
| pH | 10 | 10 | 4 | 4 |
| 溶液 | 氨水 | NaOH溶液 | 醋酸 | 盐酸 |
| A. | 若①②③④四种溶液等体积混合,混合液pH=7,则混合液中c(NH4+)=c(CH3COO-) | |
| B. | ①④两溶液等体积混合,混合液中c(H+)>c(OH-) | |
| C. | ①③溶液中水的电离程度相等 | |
| D. | V1L②和V2L④溶液混合后溶液pH=9,则V1=$\frac{11}{9}$V2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
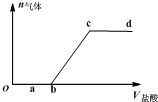 向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )
向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如图.则下列离子组在对应的溶液中一定能大量共存的是( )| A. | a点对应溶液中:Ca2+、Mg2+、Br-、NO3- | |
| B. | b点对应溶液中:Al3+、Fe3+、MnO4-、NO3- | |
| C. | c点对应溶液中:Na+、Ca2+、NO3-、Cl- | |
| D. | d点对应溶液中:F-、NO3-、Fe2+、Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 甲中试剂 | 乙中试剂 | 气体成份及实验目的 | 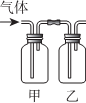 |
| A | NaHSO3溶液 | 硅酸钠溶液 | HCl:证明非金属Cl>S>Si | |
| B | FeI2淀粉溶液 | FeI2、KSCN溶液 | Cl2:验证氧化性Cl2>Fe3+>I2 | |
| C | 溴水 | AgNO3溶液 | 乙烯:验证溴水与乙烯发生的是加成反应 | |
| D | Ba(OH)2溶液 | 品红溶液 | 验证混合气体中含有SO2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
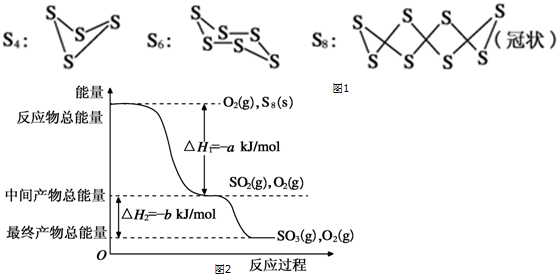
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com