
| A. | 丁烷的球棍模型 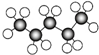 | B. | 乙烯的比例模型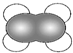 | ||
| C. | 乙醛的结构简式CH3COH | D. | 键线式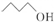 表示的有机物名称为1-戊醇 表示的有机物名称为1-戊醇 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 | NaCl |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 | 801 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
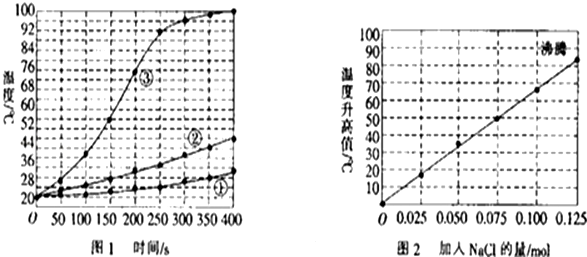
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100g氨水中含10gNH3•H2O | B. | 10gNH3溶于水形成100g溶液 | ||
| C. | 100g氨水中含10gNH3 | D. | 10gNH3溶于100gH2O形成的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入到BaCl2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ | |
| B. | 浓H2SO4与硫化亚铁制取H2S气体:H2SO4+FeS=Fe2++SO42-+H2S↑ | |
| C. | SO2使溴水褪色:SO2+2H2O+Br2=4H++SO42-+2Br- | |
| D. | 氯化铵固体与熟石灰共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝的原子失电子能力比镁强 | B. | 氟的氢化物很稳定 | ||
| C. | 水比硫化氢稳定 | D. | 氢氧化钠比氢氧化镁的碱性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
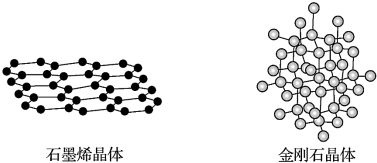
| A. | 在石墨烯晶体中,每个C原子连接3个六元环 | |
| B. | 在石墨烯晶体中,每个六元环占有3个C原子 | |
| C. | 在金刚石晶体中,C原子所连接的最小环为六元环,每个7C原子连接12个六元环 | |
| D. | 在金刚石晶体中,六元环中最多有4个C原子在同一平面 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com