
| A. | 通入氢气的电极为原电池的正极 | |
| B. | 两极材料都用石墨,用稀盐酸做电解质溶液 | |
| C. | 电解质溶液中的阳离子向通氯气的电极移动 | |
| D. | 通氯气的电极反应式为Cl2+2e-═2Cl- |
分析 A、通氢气的电极发生失去电子的氧化反应;
B、根据原电池的工作原理知识是来判断;
C、原电池中电解质溶液中的阳离子向正极移动;
D、氯气发生得电子的还原反应.
解答 解:根据燃料电池的工作原理,利用原电池原理直接制盐酸的方程式为:H2+Cl2=2HCl,该原电池的工作原理和燃料电池的工作原理相似.
A、反应H2+Cl2=2HCl中,氢气失电子,所以通入氢气的电极为原电池的负极,故A错误;
B、两极材料可以都用石墨,一极通入氢气,一极通入氯气,可以用稀盐酸做电解质溶液,故B正确;
C、在原电池中,电解质溶液中的阳离子向正极移动,通氯气的电极为正极,故C正确;
D、通氯气的电极为正极,发生得电子得还原反应,电极反应式为:Cl2+2e-=2Cl-,故D正确.
故选A.
点评 本题考查学生原电池中燃料电池的工作原理知识,注意知识的迁移和应用,是一道信息迁移题目,难度不大.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:高中化学 来源: 题型:选择题
| A. | 甲烷和乙烯:分别通入酸性KMnO4溶液 | |
| B. | 苯和四氯化碳:分别与水混合、振荡、静置 | |
| C. | 乙醇和乙酸:分别滴加NaOH溶液 | |
| D. | 棉花织品和羊毛织品:分别燃烧闻气味 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
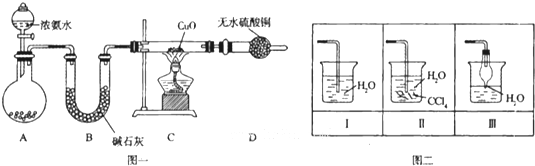
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 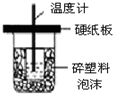 如图装置用于中和热的测定 | |
| B. | 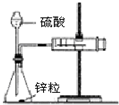 如图装置用于测定氢气的反应速率(单位mL/s) | |
| C. | 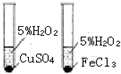 如图装置用于研究催化剂Cu2+和Fe3+对反应速率的影响 | |
| D. | 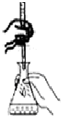 如图装置用于已知浓度的高锰酸钾溶液测定未知浓度的草酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
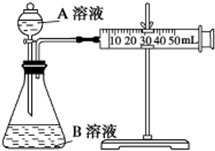 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.| 序号 | A溶液 | B溶液 |
| ① | 2mL 0.1mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ② | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液 |
| ③ | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4酸性溶液和少量MnSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Q | X | Y | ||
| M | W | Z |
| A. | 相同条件下,Q元素最低价简单氢化物是同主族元素中氢化物沸点最高的 | |
| B. | 物质W3X4中,每个原子最外层均达到8电子稳定结构 | |
| C. | X、Q、Y和氢形成的化合物中可能既有离子键、又有共价键 | |
| D. | 将Q的最高价氧化物分别通入W的盐溶液和M的盐溶液中均可产生白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com