
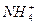 ��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�����������ֹ�ϵ��
��Cl-�������ӣ�ijͬѧ�Ʋ�������Ũ�ȴ�С˳�����������ֹ�ϵ��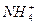 ����c��H+����c��OH-����c��Cl-����c��
����c��H+����c��OH-����c��Cl-����c��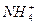 ����c��OH-����c��H+��
����c��OH-����c��H+��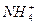 ����c��Cl-����c��OH-����c��H+����c��Cl-����c��H+����c��
����c��Cl-����c��OH-����c��H+����c��Cl-����c��H+����c��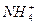 ����c��OH-��
����c��OH-��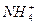 ��������ˮ�ⷴӦ
��������ˮ�ⷴӦ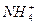 +H2O
+H2O NH3��H2O+H+��c��
NH3��H2O+H+��c��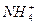 ����С��c��H+����c��OH-��������Һ��c��Cl-����c��
����С��c��H+����c��OH-��������Һ��c��Cl-����c��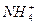
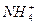 ����c��H+����c��OH-����
����c��H+����c��OH-����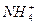 ����c��Cl-����c��OH-����c��H+������c��OH-����c��H+����֪��Һ�ʼ��ԣ�����Һ����NH4Cl��NH3��H2O��϶��ã�������ΪNH4Cl��NH3��H2O������Һ�д���c��Cl-����c��H+����c��
����c��Cl-����c��OH-����c��H+������c��OH-����c��H+����֪��Һ�ʼ��ԣ�����Һ����NH4Cl��NH3��H2O��϶��ã�������ΪNH4Cl��NH3��H2O������Һ�д���c��Cl-����c��H+����c��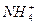 ����c��OH-������c��H+����c��
����c��OH-������c��H+����c��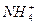 ����֪��Һ�����Դ��ڴ�NH4Cl��Һ�����ԣ�����Һ����NH4Cl�������϶��á�
����֪��Һ�����Դ��ڴ�NH4Cl��Һ�����ԣ�����Һ����NH4Cl�������϶��á�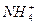 ��=c��Cl-��n��
��=c��Cl-��n��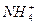 ��=n��Cl-��������Һ����δ��Ӧ��NH3��H2O������ǰn��NH3��H2O����n��HCl��c��NH3��H2O����c��HCl����
��=n��Cl-��������Һ����δ��Ӧ��NH3��H2O������ǰn��NH3��H2O����n��HCl��c��NH3��H2O����c��HCl����

 ���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
���ɶ���ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
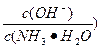 ��ֵ_________(�������С�����䡱)��
��ֵ_________(�������С�����䡱)���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 )֮�ȸ��ӽ�2��1�Ĵ�ʩ�ǣ���
)֮�ȸ��ӽ�2��1�Ĵ�ʩ�ǣ���| A����ˮ | B����NaOH���� |
| C����KOH���� | D������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 )�����ǣ���
)�����ǣ���| A��NH4HSO4 | B��NH4HCO3 | C��CH3COONH | D��NH4Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��c�� ����c��Cl-����c��H+����c��OH-�� ����c��Cl-����c��H+����c��OH-�� |
B��c�� ��=c��Cl-����c��H+����c��OH-�� ��=c��Cl-����c��H+����c��OH-�� |
C��c��Cl-����c�� ����c��H+����c��OH-�� ����c��H+����c��OH-�� |
D��c��Cl-����c��OH-����c�� ����c��H+�� ����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������� | B������NaOH��Һ | C������KOH��Һ | D������KHS��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NH3��H2O |
| B��MgO |
| C��Na2CO3 |
| D��NaOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2PO4-��Na+��Cl-��OH- | B��Al3+��Na+��HCO3-��SO42- |
| C��H+��Fe2+��NO3-��SO42- | D��Na+��NH4+��HCO3-��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H+)��c(OH-) | B��c(HCN)��c(CN-)=0.2mol/L |
| C��c(HCN)��c(CN-) | D��c(CN-)��c(OH-)=0.1mol/L |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com