
| A. | 0.1molNa与O2在一定条件下生成Na2O和Na2O2混合物时,失去电子数为0.2NA | |
| B. | 50mL 12mol•L-1浓盐酸与足量二氧化锰加热反应,生成Cl2的分子数为0.15NA | |
| C. | 常温下,100mL 1mol•L-1Na2CO3溶液中阴离子总数等于0.1NA | |
| D. | 标准状况下,6.72LCO2中所含的共用电子对数为1.2NA |
分析 A.Na元素的化合价由0升高为+1价;
B.n(HCl)=0.05L×12mol/L=0.6mol,由4HCl~Cl2可知,完全反应生成0.15mol气体,但随反应进行,浓盐酸变为稀盐酸,稀盐酸与二氧化锰不反应;
C.碳酸根离子水解生成碳酸氢根离子和氢氧根离子,阴离子增多;
D.n(CO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,CO2结构式为O=C=O,结合N=nNA计算.
解答 解:A.Na元素的化合价由0升高为+1价,则0.1molNa与O2在一定条件下生成Na2O和Na2O2混合物时,失去电子数为0.1NA,故A错误;
B.n(HCl)=0.05L×12mol/L=0.6mol,由4HCl~Cl2可知,完全反应生成0.15mol气体,但随反应进行,浓盐酸变为稀盐酸,稀盐酸与二氧化锰不反应,则生成Cl2的分子数小于0.15NA,故B错误;
C.碳酸根离子水解生成碳酸氢根离子和氢氧根离子,阴离子增多,则常温下,100mL 1mol•L-1Na2CO3溶液中阴离子总数大于0.1NA,故C错误;
D.n(CO2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,CO2结构式为O=C=O,由N=nNA可知,标准状况下,6.72LCO2中所含的共用电子对数为0.3mol×4×NA=1.2NA,故D正确;
故选D.
点评 本题考查物质的量的计算及阿伏伽德罗常数,为高频考点,把握物质的量计算公式、盐类水解及氧化还原反应等为解答的关键,综合性较强,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:
A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
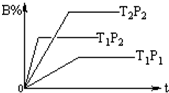 已知某可逆反应:mA(g)+nB(g)═fC(g),在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)═fC(g),在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是( )| A. | T2>T1 P1>P2 m+n>f△H<0 | B. | T1>T2 P1<P2 m+n<f△H>0 | ||
| C. | T1<T2 P1<P2 m+n<f△H<0 | D. | T1>T2 P1<P2 m+n>f△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L溶液中含Ba2+、N${O}_{3}^{-}$的总数是0.6NA | |
| B. | 500 mL溶液中Ba2+的浓度是0.2 mol•L-1 | |
| C. | 500 mL溶液中N${O}_{3}^{-}$的浓度是0.2 mol•L-1 | |
| D. | 1 L溶液中含有0.4NA个N${O}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 砹(第ⅦA)是一种有色固体,它的气态氰化物很不稳定,砹化银为有色沉淀,且不溶解于稀硝酸,但是容易分解 | |
| B. | 在周期表中金属和非金属元素的分界线附件可以寻找制取新农药的元素 | |
| C. | 铷的硫酸盐易溶解于水,其氢氧化物一定是强碱 | |
| D. | 溴化氢没有氯化氢稳定,其水溶液的酸性比较为:盐酸>氢溴酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验目的 |
| A | 将二氧化硫气体通入紫色石蕊试液中,观察溶液颜色变化 | 证明二氧化碳具有漂白性 |
| B | 向2mL1mol•L-1NaOH溶液中先加入3滴1mol•L-1FeCl3溶液,再加入3滴1mol•L-1MgCl2溶液 | 证明Ksp[Mg(OH)2]>ksp[Fe(OH)3] |
| C | 向2mL品红溶液和2mL加入少许醋酸的品红溶液中分别滴入3滴含NaClO的“84”消毒液,观察红色褪色的快慢 | 证明随着溶液pH的减小,“84”消毒液的氧化能力增强 |
| D | 相同温度下,向两支盛有相同体积不同浓度H2O2溶液的试管中分别滴入适量相同浓度的CuSO4溶液和FeCl3溶液 | 探究Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn2+、Fe2+和Cu2+ | B. | Zn2+、Fe3+和Cu2+ | C. | Fe2+和Zn2+ | D. | Cu2+ 和Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大力发展火力发电,解决电力紧张问题 | |
| B. | 在屋顶安装太阳能热水器为居民提供生活用热水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须回收处理 | |
| D. | 用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、HCO3-、MnO4- | B. | Al3+、Mg2+、HCO3- | ||
| C. | Al3+、Mg2+、SO42- | D. | Al3+、Mg2+、NH4+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com