
【题目】下列离子方程式中正确的是( )
A.碳酸氢铵溶液加足量氢氧化钠并加热:NH4++OH﹣ ![]() H2O+NH3↑
H2O+NH3↑
B.Na218O2加入H2O中:2Na218O2+2H2O═4Na++4OH﹣+18O2↑
C.硫酸镁溶液加氨水:Mg2++2NH3?H2O═Mg(OH)2↓+2NH4+
D.氧化亚铁溶于稀硝酸:FeO+2H+═Fe2++H2O
科目:高中化学 来源: 题型:
【题目】下图是研究二氧化硫性质的微型实验装置。现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不污染空气。下列说法中错误的是( )
A.紫色石蕊溶液变蓝色
B.品红溶液褪色
C.溴水的橙色褪去
D.含酚酞的NaOH溶液红色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下表中各项的排布规律,按此规律排布第30项应为( )
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 | C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
A. C8H18 B. C8H16O2 C. C9H20 D. C9H20O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是。
(2)该反应中,发生还原反应的过程是→。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目:。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( ) 
A.该反应属于氧化还原反应
B.甲和丙中同种元素化合价不可能相等
C.丁物质一定是非金属单质
D.配平后甲、乙、丙的化学计量数均为2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机化合物的同分异构体数目最多的是( )
A.分子式为C5H10O2的酯类
B.分子式为C5H10的烯烃
C.分子式为C5H12O的醇类
D.分子式为C5H12的所有化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图甲、乙两种化合物的结构或性质描述正确的是( ) 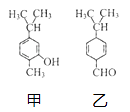
A.甲和乙互为同分异构体,均既能发生氧化反应,又能发生酯化反应
B.分子中共平面的碳原子数相同
C.可用红外光谱区分,但不能用核磁共振氢谱区分
D.均能与溴水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答下列问题:
(1)31Ga基态原子的核外电子排布式是 , 某种半导体材料由Ga和As两种元素组成,该半导体材料的化学式是 , 其晶体结构类型可能为 .
(2)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构式如图所示:以下关于维生素B1的说法正确的是 . 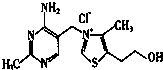
a.只含σ键和π键
b.既有共价键又有离子键
c.该物质的熔点可能高于NaCl
d.既含有极性键又含有非极性键
(3)维生素B1晶体溶于水的过程中要克服的微粒间的作用力有 .
A.离子键、共价键
B.离子键、氢键、共价键
C.氢键、范德华力
D.离子键、氢键、范德华力.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾(FeSO47H2O)是治疗缺铁性贫血药品的重要成分.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法: 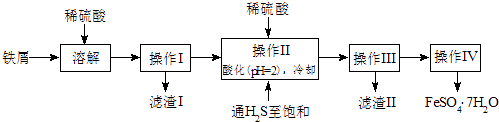
已知:室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
(1)操作II中,通入硫化氢至饱和的目的是;在溶液中用硫酸酸化至pH=2的目的是 .
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质,② .
(3)测定绿矾产品中Fe2+含量的方法是:a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL. ①滴定时发生反应的离子方程式为: .
②滴定时盛放KMnO4溶液的仪器为(填仪器名称).判断此滴定实验达到终点的方法是
③计算上述样品中FeSO47H2O的质量分数为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com