
【题目】实验室常用热的氢氧化钠溶液洗去试管内壁沾有的硫单质,发生反应6NaOH+3S![]() 2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
2Na2S+Na2SO3+3H2O。关于该反应的说法不正确的是( )
A. 硫既是氧化剂又是还原剂 B. 硫化钠是还原产物
C. 硫既表现氧化性又表现还原性 D. 消耗3 mol 硫,转移电子6 mol
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】按题给要求填空
(1)某烷烃1分子含有50个电子,该烷烃只能由一种结构的炔烃加氢得到,则该烷烃的结构简式为_________________或_________________ 。
(2)分子式为C6H12 的某烃的所有碳原子都在同一平面上,则该烃的结构简式为_____________________________,若分子式为C4H6的某烃中所有的碳原子都在同一条直线上,则该烃的结构简式为_____________________________________。
(3)写出以乙炔为原料制备聚氯乙烯反应方程式(无机物不限)
①___________________________________________________。
②___________________________________________________。
(4)下列卤代烃在 KOH 醇溶液中加热不反应的是_____________________(填序号)。
①![]() ②(CH3)2CHCH2Cl ③
②(CH3)2CHCH2Cl ③![]() ④CHCl2CH2Br
④CHCl2CH2Br
⑤(CH3)3CCH2Cl ⑥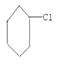 ⑦CH2=CHCl
⑦CH2=CHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中Cl-浓度最小的是 ( )
A.250mL 1mol/L AlCl3溶液B.200mL 2mol/L MgCl2溶液
C.1L 2.5mol/L NaCl溶液D.300mL 5mol/L KClO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂。可通过反应获得:2NO(g)+Cl2(g) ![]() 2ClNO(g)
2ClNO(g)
(1)氢氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) ![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s) ![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g) ![]() 2ClNO(g) K3
2ClNO(g) K3
则K3=______________(用K1和K2表示)。
(2)按投料比[n(NO):n(Cl2)=2:1]把NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强P(总压)的关系如图A所示:
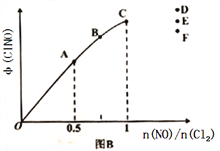
①该反应的△H______0(填“>”“<”或“=”);
②在P压强条件下,M点时容器内NO的体积分数为_________;
③若反应一直保持在P压强条件下进行,则M点的分压平衡常数Kp=__________(用含P的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
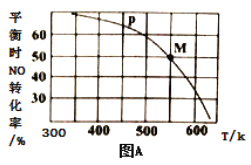
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数的变化图像如图B,则A、B、C三状态中,NO的转化率最大的是_________点;当n(NO)/n(Cl2)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_____________点。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2+是一种非常好的还原剂,能够与很多氧化剂发生反应。
(1)在加热条件下,FeSO4可与硫酸酸化的KNO3反应,其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NO气体。
①请写出该化学反应方程式,并用单线桥表示出电子转移的方向和数目_________________。
②上述反应发生还原反应的物质是______________ 。
③若11.4gFeSO4参与反应,则产生NO气体的体积(标况下)___________L。
(2)难溶物FeS能够与硫酸酸化的KMnO4溶液反应,反应方程式如下:
10FeS+6KMnO4+24H2SO4=3K2SO4+6MnSO4+5Fe2(SO4)3+l0 +24H2O
①横线上的物质的化学式是___________。
②该反应的氧化产物是______________。
③若上述反应前后固体的质量减少了2.8g,则硫元素与KMnO4之间发生转移的电子数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H可用以下路线合成:
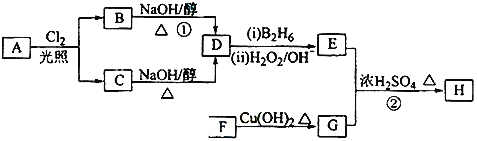
已知:![]()
回答下列问题:
(1)11.2L(标准状况)的烃A在氧气中充分燃烧可以生成88g CO2和45g H2O,且A分子结构中有3个甲基,则A的结构简式为______________;
(2)B和C均为一氯代烃,D的名称(系统命名)为_______________;
(3)在催化剂存在下1mol F与2mol H2反应,生成3﹣苯基﹣1﹣丙醇.F的结构简式 是_________________________________________________________________________;
(4)反应①的反应类型是_________________________________________________________;
(5)反应②的化学方程式为______________________________________________________;
(6)写出与G具有相同官能团的芳香类的G的同分异构体的结构简式___________________.(任写一种。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】简单原子的原子结构可用下图形象地表示:
![]()
其中“●”表示质子或电子,“○”表示中子,则下列有关①②③的叙述正确的是( )
A. ①②③是三种不同的氢分子B. ①②③互为同位素
C. ①②③是三种化学性质不同的粒子D. ①②③具有相同的质量数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单元为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
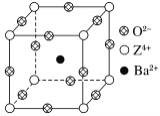
(1) Y在周期表中位于______________;Z4+的核外电子排布式为___________________。
(2)X的该种氢化物分子构型为________,X在该氢化物中以_______方式杂化。X和Y形成的化合物的熔点应该_______(填“高于”或“低于”)X氢化物的熔点。
(3)①制备M的化学方程式是_____________。
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的________。
③在M晶体中,Z4+的氧配位数为________。
④已知O2-半径为1.40×10-10 m,则Z4+半径为____ m。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com