
已知:2HI+Cl2===2HCl+I2,I2为固体。常温常压下,两个容积相同的烧瓶中分别盛满X和Y两种气体,打开开关a,两烧瓶内的气体充分混合后,容器内的压强由大到小的顺序正确的是 ( )
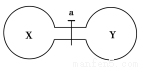
A.②>③>①>④ B.③>①=④>②
C.③>①>④>② D.④>①>②>③
科目:高中化学 来源:2015-2016学年贵州省高二上学期期末化学试卷(解析版) 题型:实验题
现用物质的量浓度为a mol·L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
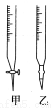
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是________________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入________(填“甲”或“乙”)中。
(3)如图是碱式滴定管中液面在滴定前后的读数,c(HCl)________mol·L-1。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:填空题
甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)===2H2O(l) ΔH1=-571.8kJ/mol;
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH2=-192.9kJ/mol
(1)甲醇蒸气完全燃烧的热化学方程式为_____________________________。
(2)反应②中的能量变化如图所示,则ΔH2=_________________________。
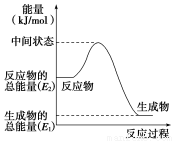
(3)H2(g)的燃烧热为____________________。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上期末考试化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、U原子序数依次递增。X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13。Y元素的单质在X的某种氧化物中可燃。下列说法正确的是
A.X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X
B.Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡
C.Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U
D.室温下,0.05 mol/L U的气态氢化物的水溶液的pH>1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期末考试化学试卷(解析版) 题型:选择题
在①丙烯(CH2=CH—CH3);②氯乙烯;③苯;④甲苯( 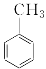 )四种有机物中,分子内所有原子均在同一平面的是
)四种有机物中,分子内所有原子均在同一平面的是
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上期末考试化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.0.1 mol/LCH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上期末(理)化学试卷(解析版) 题型:选择题
下列物品或设备:①工业制粗硅 ②门窗玻璃 ③水晶项链 ④石英钟表 ⑤玛瑙手镯 ⑥硅太阳能电池⑦光导纤维 ⑧计算机芯片 。所用材料为SiO2或要用到SiO2的是
A.①②③④⑤⑦ B.全部 C.③④⑤⑦⑧ D.①②⑦⑧
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三上一轮复习检测一化学试卷(解析版) 题型:选择题
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)
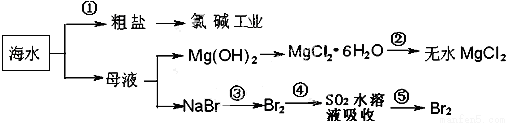
下列有关说法不正确的是( )
A.从能量转换角度来看,框图中的氯碱工业是一个将电能转化为化学能量的过程
B.过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2
C.在过程③⑤中溴元素均被氧化
D.过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+ 等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江省高二上期末化学试卷(解析版) 题型:选择题
已知:H2(g)+I2(g)  2HI(g) △H < 0 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各 0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
2HI(g) △H < 0 有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各 0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
A.甲、乙提高相同温度 B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变 D.甲增加0.1 mol H2,乙增加0.1 mol I2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com