
| Ń”Ļī | ²Ł×÷ | ĻÖĻó | ½įĀŪ |
| A | ³£ĪĀĻĀ½«Cuʬ·ÅČėÅØH2SO4ÖŠ | Éś³É“Ģ¼¤ŠŌĘųĪ¶ĘųĢå | CuÓėÅØH2SO4·“Ӧɜ³ÉSO2 |
| B | Al2£ØSO4£©3ČÜŅŗÖŠµĪ¼Ó¹żĮæ°±Ė® | Éś³É°×É«½ŗדĪļÖŹ | Al£ØOH£©3²»ČÜÓŚ°±Ė® |
| C | ĻņijČÜŅŗÖŠ¼ÓČėKSCNČÜŅŗ£¬ŌŁĻņČÜŅŗÖŠ¼ÓČėŠĀÖĘĀČĖ® | ČÜŅŗĻČ²»ĻŌŗģÉ«£¬¼ÓČėĀČĖ®ŗó±äŗģÉ« | øĆČÜŅŗÖŠŗ¬ÓŠFe2+ |
| D | ĻņijČÜŅŗÖŠ¼ÓČėCCl4£¬Õńµ“ŗó¾²ÖĆ | ŅŗĢå·Ö²ć£¬ĻĀ²ć³Ź×ĻŗģÉ« | øĆČÜŅŗÖŠ“ęŌŚI- |
| AӢA | BӢB | CӢC | DӢD |


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢“¢“ęŅŗĀȵÄøÖĘæ·¢ÉśŠ¹Ā©£¬Į¢¼“ĻņæÕÖŠÅēČ÷±„ŗĶŹ³ŃĪĖ® |
| B”¢ŹµŃéŹŅÖŠÄĘ×Å»š£¬Į¢¼“ÓĆÅŻÄĆš»šĘ÷Ćš»š |
| C”¢ÅØĮņĖį²»É÷Õ“ŌŚŹÖÉĻ£¬Į¢¼“ÓĆ“óĮæµÄĖ®³åĻ“£¬ŌŁĶæÉĻĒāŃõ»ÆÄĘÅØČÜŅŗ |
| D”¢ŹµŃéŹŅ³£½«Įņ»ĒČöŌŚ¹ÆµÄ±ķĆę£¬ŅŌ³żČ„²»É÷Č÷ĀäµÄ¹Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ĻĀ±ķŹĒŌŚ0.1MPaĻĀ£¬²»Ķ¬ĪĀ¶ČŹ±£¬¶žŃõ»ÆĮņ“ß»ÆŃõ»Æ³ÉČżŃõ»ÆĮņµÄĘ½ŗā×Ŗ»ÆĀŹ£ØŌĮĻĘų³É·ÖµÄĢå»ż·ÖŹż£ŗSO27%£¬O211%£¬N282%£©£ŗ
ĻĀ±ķŹĒŌŚ0.1MPaĻĀ£¬²»Ķ¬ĪĀ¶ČŹ±£¬¶žŃõ»ÆĮņ“ß»ÆŃõ»Æ³ÉČżŃõ»ÆĮņµÄĘ½ŗā×Ŗ»ÆĀŹ£ØŌĮĻĘų³É·ÖµÄĢå»ż·ÖŹż£ŗSO27%£¬O211%£¬N282%£©£ŗ| ĪĀ¶Č/”ę | 400 | 450 | 475 | 500 | 525 | 575 |
| ×Ŗ»ÆĀŹ/% | 99.2 | 97.5 | 95.8 | 93.5 | 90.5 | 79.9 |
| ŹµŃé ±ąŗÅ |
Ń¹Ēæ£ØMPa£© | SO2³õŹ¼Ģå»ż·ÖŹż £Ø%£© |
O2³õŹ¼Ģå»ż·ÖŹż £Ø%£© |
N2³õŹ¼Ģå»ż·ÖŹż £Ø%£© |
| ¢ń | 0.1 | 7% | 11% | 82% |
| ¢ņ | ¢Ł | 7% | 15% | ¢Ś |
| ¢ó | 0.5 | ¢Ū | 15% | ¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ŹµŃé×é | ĪĀ¶Č/”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | ||
| CO | H2O | H2 | CO | ||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢0.1mol?L-1°±Ė®£¬ČÜŅŗµÄpH=13 |
| B”¢0.1mol?L-1°±Ė®¼ÓĖ®Ļ”ŹĶ£¬ČÜŅŗÖŠc£ØH+£©ŗĶc£ØOH-£©¶¼¼õŠ” |
| C”¢0.1mol?L-1“×ĖįČÜŅŗÖŠ£ŗc£ØH+£©=c£ØCH3COO-£© |
| D”¢0.1mol?L-1“×ĖįÓė0.1mol?L-1 NaOHČÜŅŗµČĢå»ż»ģŗĻĖłµĆČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØCH3COO-£©£¾c£ØOH-£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ĆĄ¹śŹ„Ā·Ņ×Ė¹“óѧъÖĘŠĀŠĶµÄŅŅ“¼Č¼ĮĻµē³Ų£¬ÓĆÖŹ×Ó£ØH+£©ČܼĮ£¬ŌŚ200”ę×óÓŅ¹©µē£®µē³Ų×Ü·“Ó¦ĪŖ£ŗC2H5OH+3O2”ś2CO2+3H2O£¬ČēĶ¼ŹĒøƵē³ŲµÄŹ¾ŅāĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
ĆĄ¹śŹ„Ā·Ņ×Ė¹“óѧъÖĘŠĀŠĶµÄŅŅ“¼Č¼ĮĻµē³Ų£¬ÓĆÖŹ×Ó£ØH+£©ČܼĮ£¬ŌŚ200”ę×óÓŅ¹©µē£®µē³Ų×Ü·“Ó¦ĪŖ£ŗC2H5OH+3O2”ś2CO2+3H2O£¬ČēĶ¼ŹĒøƵē³ŲµÄŹ¾ŅāĶ¼£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A”¢a¼«ĪŖµē³ŲµÄÕż¼« |
| B”¢µē³Ų¹¤×÷Ź±µēĮ÷ÓÉa¼«ŃŲµ¼Ļß¾µĘÅŻŌŁµ½b¼« |
| C”¢µē³ŲÕż¼«µÄµē¼«·“Ó¦ĪŖ£ŗ4H++O2+4e-ØT2H2O |
| D”¢µē³Ų¹¤×÷Ź±£¬1molŅŅ“¼±»Ńõ»ÆŹ±¾ĶÓŠ6molµē×Ó×ŖŅĘ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢±łŗĶĖ® |
| B”¢ŃõĘųŗĶ³ōŃõ |
| C”¢1HÓė3H |
| D”¢CH3CH20HŗĶCH30CH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
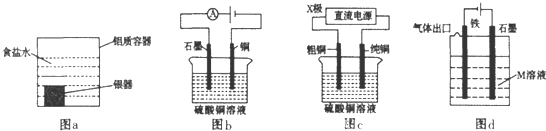
| A”¢ĄūÓĆĶ¼a×°ÖĆ“¦ĄķŅųĘ÷±ķĆęµÄŗŚ°ßAg2S£¬ŅųĘ÷±ķĆę·¢ÉśµÄ·“Ó¦ĪŖAg2S+2e-=2Ag+S2- |
| B”¢Ķ¼bµē½āŅ»¶ĪŹ±¼ä£¬Ķµē¼«Čܽā£¬ŹÆÄ«µē¼«ÉĻÓŠĮĮŗģÉ«ĪļÖŹĪö³ö |
| C”¢Ķ¼cÖŠµÄX¼«ČōĪŖøŗ¼«£¬ŌņøĆ×°ÖĆæÉŹµĻÖ“ÖĶµÄ¾«Į¶ |
| D”¢Ķ¼dÖŠČōMŹĒŗ£Ė®£¬øĆ×°ÖĆŹĒĶعż”°ĪžÉüŃō¼«µÄŅõ¼«±£»¤·Ø”±Ź¹Ģś²»±»øÆŹ“ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com