
 ŌŖĖŲX»łĢ¬Ō×ÓŗĖĶāµē×ÓŹżĪŖ29£¬ŌŖĖŲYĪ»ÓŚXµÄĒ°Ņ»ÖÜĘŚĒŅ×īĶā²ćµē×ÓŹżĪŖ1£¬ŌŖĖŲZ»łĢ¬Ō×Ó3p¹ģµĄÉĻÓŠ4øöµē×Ó£¬ŌŖĖŲPŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ3±¶£¬ŌŖĖŲQ»łĢ¬Ō×Ó2p°ė³äĀś£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŌŖĖŲX»łĢ¬Ō×ÓŗĖĶāµē×ÓŹżĪŖ29£¬ŌŖĖŲYĪ»ÓŚXµÄĒ°Ņ»ÖÜĘŚĒŅ×īĶā²ćµē×ÓŹżĪŖ1£¬ŌŖĖŲZ»łĢ¬Ō×Ó3p¹ģµĄÉĻÓŠ4øöµē×Ó£¬ŌŖĖŲPŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµē×ÓŹżµÄ3±¶£¬ŌŖĖŲQ»łĢ¬Ō×Ó2p°ė³äĀś£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ·ÖĪö ŌŖĖŲX»łĢ¬Ō×ÓŗĖĶāµē×ÓŹżĪŖ29£¬ŌņXĪŖCu£¬ŌŖĖŲYĪ»ÓŚXµÄĒ°Ņ»ÖÜĘŚ¼“µŚČżÖÜĘŚ£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖ1£¬ŌņYĪŖNa£¬ŌŖĖŲZ»łĢ¬Ō×ÓµÄ3p¹ģµĄÉĻÓŠ4øöµē×Ó£¬ŌņZŹĒSŌŖĖŲ£»ŌŖĖŲPµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµÄ3±¶£¬ŌŖĖŲ×īĶā²ćµē×ÓŹżŠ”ÓŚ»ņµČÓŚ8£¬ĖłŅŌPŹĒOŌŖĖŲ£¬ŌŖĖŲQ»łĢ¬Ō×Ó2p°ė³äĀś£¬ŌņQĪŖN£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗŌŖĖŲX»łĢ¬Ō×ÓŗĖĶāµē×ÓŹżĪŖ29£¬ŌņXĪŖCu£¬ŌŖĖŲYĪ»ÓŚXµÄĒ°Ņ»ÖÜĘŚ¼“µŚČżÖÜĘŚ£¬ĒŅ×īĶā²ćµē×ÓŹżĪŖ1£¬ŌņYĪŖNa£¬ŌŖĖŲZ»łĢ¬Ō×ÓµÄ3p¹ģµĄÉĻÓŠ4øöµē×Ó£¬ŌņZŹĒSŌŖĖŲ£»ŌŖĖŲPµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäÄŚ²ćµÄ3±¶£¬ŌŖĖŲ×īĶā²ćµē×ÓŹżŠ”ÓŚ»ņµČÓŚ8£¬ĖłŅŌPŹĒOŌŖĖŲ£¬ŌŖĖŲQ»łĢ¬Ō×Ó2p°ė³äĀś£¬ŌņQĪŖN£¬
£Ø1£©XĪŖCu£¬X»łĢ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ1s22s22p63s23p63d104s1£¬
¹Ź“š°øĪŖ£ŗ1s22s22p63s23p63d104s1£»
£Ø2£©QĪŖN£¬QµÄĘųĢ¬Ēā»ÆĪļĪŖ°±£¬°±·Ö×ÓÖŠµŖŌ×ӵļŪ²ćµē×Ó¶ŌŹżĪŖ$\frac{5+3}{2}$=4£¬ĖłŅŌ¹ģµĄŌÓ»ÆĄąŠĶŹĒsp3£¬·Ö×ÓÖŠÓŠŅ»¶Ō¹Āµē×Ó¶Ō£¬øĆ·Ö×ÓµÄæռ乹ŠĶĪŖČż½Ē׶ŠĪ£¬
¹Ź“š°øĪŖ£ŗsp3£»Čż½Ē׶£»
£Ø3£©PŹĒOŌŖĖŲ£¬QĪŖN£¬ÓÉÓŚµŖŌ×ÓµÄ×īĶā²ćŹĒ°ė³äĀś×“Ģ¬£¬ŹĒŅ»ÖÖĪČ¶Ø½į¹¹£¬ĖłŅŌOÓėNµÄµŚŅ»µēĄėÄܵē󊔹ŲĻµĪŖN£¾O£¬
¹Ź“š°øĪŖ£ŗN£¾O£»
£Ø4£©ZŹĒSŌŖĖŲ£¬ŹĒOŌŖĖŲ£¬Įņ»ÆĒāÓėŅŅ“¼²»ÄÜŠĪ³ÉĒā¼ü£¬¶ųĖ®ÄÜÓėŅŅ“¼ŠĪ³ÉĒā¼ü£¬ĖłŅŌĮņ»ÆĒāŌŚŅŅ“¼ÖŠµÄČܽā¶ČŠ”ÓŚYĖ®ŌŚŅŅ“¼ÖŠµÄČܽā¶Č£¬
¹Ź“š°øĪŖ£ŗH2OÓėŅŅ“¼·Ö×Ó¼äŠĪ³ÉĒā¼ü£»
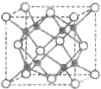
£Ø5£©YĪŖNa£¬PŹĒOŌŖĖŲ£¬ÄĘÓėŃõŠĪ³ÉµÄ»ÆŗĻĪļµÄŅõŃōĄė×ÓøöŹżÖ®±ČĪŖ1£ŗ2£¬øł¾Ż¾§°ūµÄ½į¹¹Ķ¼æÉÖŖ£¬Ķ¼ÖŠæÕŠÄĒņĪŖ8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$=4£¬¶ųŹµŠÄĒņĪŖ8øö£¬ĖłŅŌæÕŠÄĒņĪŖŃõĄė×Ó£¬ŹµŠÄĒņĪŖÄĘĄė×Ó£¬ŅŌ¶„µćÉĻµÄŃõĄė×ÓĪŖĄż£¬øł¾ŻĶ¼æÉÖŖ£¬ÓėŃõĄė×Ó×ī½üµÄÄĘĄė×ÓÓŠ8øö£¬ĖłŅŌŃõĄė×ÓµÄÅäĪ»ŹżĪŖ8£¬¾§°ū²ĪŹża=0.566nm£¬øĆ¾§ĢåµÄĆܶČĪŖ$\frac{\frac{4”Į£Ø46+16£©}{{N}_{A}}g}{£Ø{0.566nm£©}^{3}}$=$\frac{4”Į62}{£Ø0.566”Į10{\;}^{-7}£©^{3}”Į6.02”Į10{\;}^{23}}$g/cm3=2.27g/cm3£¬
¹Ź“š°øĪŖ£ŗ8£»2.27£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹ÓėŠŌÖŹµÄ漲飬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢ŌÓ¾§°ū¼ĘĖć”¢Ēā¼ü”¢Ō×ÓŌӻƷ½Ź½”¢µŚŅ»µēĄėÄÜµČ£¬×¢Ņā¶Ō»ł“”ÖŖŹ¶µÄĄķ½āÕĘĪÕ£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 12ŗĶ8 | B£® | 6ŗĶ8 | C£® | 20ŗĶ9 | D£® | 11ŗĶ16 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2SeµÄČČĪČ¶ØŠŌ±Č H2SµÄĪČ¶ØŠŌĒæ | B£® | SeO3µÄĖ®»ÆĪļŹĒŅ»ÖÖŗ¬ŃõĖį | ||
| C£® | ĪųŌŖĖŲÓŠ+6”¢+4”¢-2µČ³£¼ū»ÆŗĻ¼Ū | D£® | SeµÄµ„ÖŹŌŚ³£ĪĀĻĀ³Ź¹ĢĢ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¶ĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢D”¢EµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅŌ×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ17£®AŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬BŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä“Ī×īĶā²ćµē×ÓŹżµÄ2±¶£¬AÓėEĶ¬Ö÷×壬DŌ×ÓŗĖĶāÓŠ2øöĪ“³É¶Ōµē×Ó£®
¶ĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢D”¢EµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬ĒŅŌ×Ó×īĶā²ćµē×ÓŹżÖ®ŗĶĪŖ17£®AŹĒŌŖĖŲÖÜĘŚ±ķÖŠŌ×Ó°ė¾¶×īŠ”µÄŌŖĖŲ£¬BŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä“Ī×īĶā²ćµē×ÓŹżµÄ2±¶£¬AÓėEĶ¬Ö÷×壬DŌ×ÓŗĖĶāÓŠ2øöĪ“³É¶Ōµē×Ó£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČõĖį»ÆѧŹ½ | HSCN | CH3COOH | HCN | H2CO3 |
| µēĄėĘ½ŗā³£Źż | 1.3”Į10-1 | 1.8”Į10-5 | 4.9”Į10-10 | K1=4.3”Į10-7”” K2=5.6”Į10-11 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | C2H5Br | B£® | ĀČĖ® | C£® | äåµÄCCl4ČÜŅŗ | D£® | KClO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

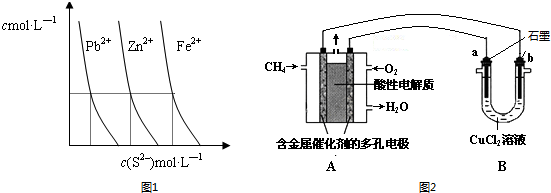
| A£® | a”¢bĮ½µćČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬ | |
| B£® | a”¢bĮ½µćČÜŅŗµÄpHĀś×ć£ŗpH£Øa£©£¾pH£Øb£© | |
| C£® | cµćČÜŅŗĀś×ć£ŗc£ØNa+£©£¾c£ØCO3 2-£©£¾c£ØOH-£©£¾c£ØHCO3-£©£¾c£ØH+£© | |
| D£® | a”¢b”¢cČżµćČÜŅŗ¶¼Āś×ć£ŗc£ØNa+£©+c£ØH+£©=c£ØHCO3-£©+2c£ØCO3 2-£©+c£ØOH-£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com