
| A、分散系只包括溶液和胶体 |
| B、电解质和非电解质构成所有的物质 |
| C、相同体积的两溶液,物质的量浓度大的溶液含有溶质的质量就越大 |
| D、单位物质的量的物质所具有的质量叫摩尔质量,摩尔质量与1mol物质的质量数值相同 |


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:
| A、CaCl2在熔融状态下可导电,它是强电解质 |
| B、没有单质参加的化合反应一定是非氧化还原反应 |
| C、元素处于最高价态时一定具有强氧化性 |
| D、在2KClO3+4HCl(浓)═2KCl+2ClO2+Cl2+2H2O中,氯气既是氧化产物又是还原产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.2mol/LNa2CO3溶液中所含CO32-的数目为0.2NA |
| B、常温常压下,5.6g乙烯与丁烯的混合物中含有的氢原子的数目为0.8NA |
| C、50mL18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、22.4LCO2与足量Na2O2充分反应,反应中转移的电子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、实验室制取氢气:Zn+H2SO4=ZnSO4+H2↑ | ||||
| B、铁丝与硫酸铜溶液反应:Fe+CuSO4=Cu+FeSO4 | ||||
| C、用稀盐酸除铁锈:Fe2O3+6HCl=2FeCl2+3H2O | ||||
D、酒精燃烧:C2H5OH+3O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
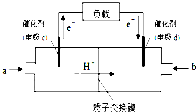

查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com