
0.1mol/L盐酸中水的电离度和由水电离出的[H+]分别为
A.1.8×10-13%、10-13mol/L
B.1.8×10-12%、10-12mol/L
C.1.5×10-13%、10-13mol/L
D.1.8×10-13%、10-12mol/L
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:022
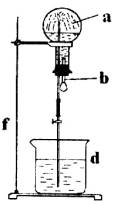 在烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是(
)
在烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是(
)
|
|
a(干燥气体) |
b(液体) |
|
(A) |
NO2 |
水 |
|
(B) |
CO2 |
4mol/LNaOH溶液 |
|
(C) |
C12 |
饱和NaCl水溶液 |
|
(D) |
NH3 |
1mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
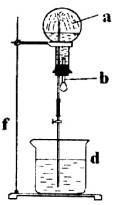 在烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是(
)
在烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是(
)
|
|
a(干燥气体) |
b(液体) |
|
(A) |
NO2 |
水 |
|
(B) |
CO2 |
4mol/LNaOH溶液 |
|
(C) |
C12 |
饱和NaCl水溶液 |
|
(D) |
NH3 |
1mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源:2010年河南省全真模拟(二)(理科综合)化学部分 题型:填空题
(15分)
(1)下列事实中,能证明亚硫酸的酸性强于氢硫酸的是 (填字母)。
a.亚硫酸受热时易分解
b.相同条件下,等浓度的亚硫酸溶液导电能力强于氢硫酸
c.亚硫酸溶液可使品红溶液褪色,而氢硫酸不能
d.常温下,浓度均为0.1mol/L的H2SO3溶液和H2S溶液的pH分别是2.1和4.5
(2)工业上除去高压锅用水中溶解的氧气常用的试剂有Na2SO3和N2H4(肼)。
①已知16g液态的肼与氧气反应得到氮气和液态水时,放热354.87kJ,该反应的热化学方程式是 。
②除去等质量的O2,所耗Na2SO3和N2H4的质量比是 (填最简整数比)。
(3)向Na2SO3和Na2S的混合溶液中加入稀盐酸,溶液中会产生大量淡黄色沉淀。则该反应中氧化剂和还原剂的物质的量之比是 。
(4)已知Na2SO3在高温下发生分解,得到两种产物。某同学称取25.2g纯净的Na2SO3·7H2O晶体在高温下隔绝空气加热至恒重,冷却后称得固体为12.6g,将其完全溶于水配成1L溶液,并测溶液的pH。
①Na2SO3高温分解的化学方程式是 。
②测得溶液的pH大于0.025mol/LNa2SO3溶液的pH,试解释原因(结合离子方程式说明) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
①水 ②NaOH溶液 ③0.1mol/L盐酸 ④0.1 mol/L硫酸铁溶液
A.④③②① B.④③①② C.③④①② D.①③④②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com