
| A、乙炔的燃烧热为1256kJ/mol |
| B、若生成2mol 液态水,则放出的热量小于2512kJ |
| C、若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
| D、若转移10mol电子,则消耗2.5molO2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
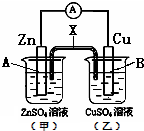
| A、若X是盐桥,则电子由B电极经外电路流向A电极 |
| B、若X是铜条,则A电极的电极反应式是:Zn2++2e-═Zn |
| C、若X是石墨条,则乙池溶液的pH会减小 |
| D、若X是锌条,则A电极的质量会增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、CH2=CH2+HCl
| |||
B、CH4+Cl2
| |||
C、2CH3CHO+O2
| |||
D、CH3CH2Br+NaOH
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、12种 | B、13种 |
| C、16种 | D、18种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是298K 时N2与H2反应过程中能量变化的曲线图.下列叙述不正确的是( )
如图是298K 时N2与H2反应过程中能量变化的曲线图.下列叙述不正确的是( )| A、该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-92kJ?mol-1 |
| B、b曲线是加入催化剂时的能量变化曲线 |
| C、加入催化剂,该化学反应的活化能和反应热都改变 |
| D、在温度体积一定的条件下,通入lmol N2和3molH2 反应后放出的热量为Q1kJ,若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2>2Q1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com