
【题目】13C—NMR(核磁共振)可用于含碳化合物的结构分析。下列有关13C的说法不正确的是( )
A. 13C的质量数是13, 核内有6个电子
B. 13C 与12C是两种不同的核素
C. 13C 与12C互为同位素
D. 13C 与12C 的化学性质有很大的差别
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】(8分)现有甲、乙、丙三名同学分别进行Fe(OH)3胶体的制备实验。
甲同学:向1 mol·L-1的FeCl3溶液中加少量NaOH溶液。
乙同学:直接加热饱和FeCl3溶液。
丙同学:向25 mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热。
试回答下列问题:
⑴其中操作正确的同学是___ _____。
⑵证明有Fe(OH)3胶体生成利用的胶体性质是______ __。
⑶在胶体中加入电解质溶液或带有相反电荷的胶体微粒能使胶体微粒沉淀出来。丁同学利用所制得的Fe(OH)3胶体进行实验:
① 将其装入U形管内,用石墨作电极,通电一段时间后发现与电源负极相连的电极区附近的颜色逐渐变深,这表明Fe(OH)3胶体微粒带__________(填“正”或“负”)电荷。
② 若向其中加入饱和Na2SO4溶液,产生的现象是 。
③若向其中加入浓盐酸溶液,产生的现象是 。
(4)Fe(OH)3胶体制备的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取7.90gKMnO4,加热分解后剩余固体7.42g。该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以Mn2+存在。
请计算:
(1)KMnO4的分解率_______________。
(2)气体A的物质的量_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。

(1)过滤所需要的主要玻璃仪器有________________________________。
(2)加入BaCl2的目的是_______________,加MgO后过滤所得滤渣的主要成分为___。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为__________________________,
再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:
①蒸发结晶;②___________;洗涤;③将滤液冷却结晶;④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定(已知Mg(ClO3)2·6H2O的摩尔质量为299g/mol )。
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00mL于锥形瓶中,加入10.00mL稀硫酸和20.00mL1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点。反应的方程式为:
______Cr2O72-+___Fe2++___ H+= ___Cr3++___Fe3++____H2O (请配平)。
步骤4:将步骤2、3重复两次,平均消耗K2Cr2O7溶液15.00 mL。
写出步骤2中发生反应的离子方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用一种试剂就可以鉴别乙酸溶液、葡萄糖溶液、蔗糖溶液,这种试剂是( )
A. NaOH溶液 B. 氢氧化铜悬浊液 C. 石蕊试液 D. 碳酸钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g铁投入200mL某浓度的盐酸中,铁和盐酸恰好完全反应。求:
(1)11.2g铁的物质的量
(2)所用盐酸中HCl的物质的量浓度
(3)反应中生成的H2在标准状况下的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】愈创木酚是香料、医药、农药等工业的重要的精细化工中间体,工业上以邻硝基氯苯为原料合成愈创木酚的一种流程如下图所示。

(1)反应①②的类型依次是_________、__________。
(2)B物质中的官能团名称是_________。
(3)C物质的分子式是__________。
(4)已知C物质水解产物之一是氮气,写出反应④的化学方程式________________。(不要求写条件)
(5)愈创木酚的同分异构体中属于芳香化合物且含有三个取代基有_______种,其中含有氢原子种类最少的物质的结构简式是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向质量分数为2a%,体积为10 mL,物质的量浓度为c1mol·L-1的稀H2SO4中加入V mL 的水,使之质量分数变为 a%,此时物质的量浓度为c2mol·L-1,则下列关系正确的是
A. V>10, 2c2=c1 B. V<10,2c2﹤c1
C. V>10,2c2<c1 D. V>10, 2c2>c1
查看答案和解析>>
科目:高中化学 来源: 题型:
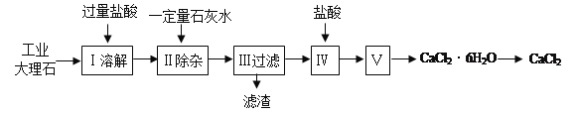
【题目】氯化钙常用于道路融冰剂和干燥剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al2O3、Fe2O3等杂质)制备氯化钙的主要流程如下:
 完成下列填空:
完成下列填空:
(1)上述使用的盐酸的物质的量浓度约为6.0mol/L,若用36.5%的盐酸(密度为1.2g/mL)配置6.0mol/L的盐酸100mL,所需的玻璃仪器有玻璃棒、量筒、胶头滴管、 ;需要量取36.5%的盐酸 mL;配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是 。
A.定容摇匀后发现液面低于刻度线 |
B.定容时俯视容量瓶的刻度线 |
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就转入定容操作 |
D.如果加水超过了刻度线,取出少量水使液面恰好到刻度线 |
(2)步骤Ⅰ中有关反应的离子方程式有: 、 、 。
(3)步骤Ⅱ控制石灰水用量的目的是防止(用离子方程式表示): 。
(4)滤渣的主要成分有(写化学式) 。
(5)步骤Ⅴ所含的操作依次是 、 。
(6)制得的氯化钙可以通过如下步骤测定其纯度:
①称取5.5g无水氯化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤;④ 、 ;⑤称量。若得到4.3g碳酸钙,则氯化钙的质量分数为 ;若实验操作规范而测定结果偏低,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com