
 电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极,且a极与电源的正极相连.以下说法错误的是( )
电解硫酸钠溶液联合生产硫酸和烧碱溶液的装置如图所示,其中阴极和阳极均为惰性电极,且a极与电源的正极相连.以下说法错误的是( )| A、同温同压下,生成气体甲与气体乙的速率比约为1:2 |
| B、产物丙为较浓的烧碱溶液 |
| C、钠离子通过离子交换膜d向b极迁移 |
| D、b电极反应式:2H2O+2e-=H2↑+2OH- |


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
| A、0.5×10-3 mol |
| B、0.8×10-3 mol |
| C、1.1×10-3 mol |
| D、1.2×10-3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
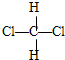 和
和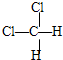 ⑦
⑦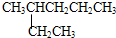 和
和 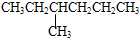
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )
如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )| A、该原电池的总反应式为2Fe3++Cu═2Fe2++Cu2+ |
| B、该电池工作时,Cu2+在电极上得到电子,发生还原反应 |
| C、该电池工作时,氯化铜溶液中氯离子浓度增大 |
| D、电池工作过程中,电子由铜电极经过电流表流向石墨电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.2 | B、1.75 |
| C、2.0 | D、2.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所用NaOH固体已潮解 |
| B、向容量瓶加水时,液面低于刻度线即摇匀 |
| C、定容时不小心加水超过了刻度线,用胶头滴管直接吸出多余部分 |
| D、有少量NaOH溶液残留在烧杯内 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com