



 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.Z的熔点较低 | B.Z可以表示为M2Y |
| C.M离子和Y离子的核外电子排布相同 | D.M形成+2价阳离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
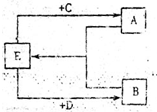
| A | | | | | |
| | | | | | B |
| c | | d | | | e |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常压下,四种元素单质中,W单质的熔点最高 |
| B.Z的阳离子与Y的阴离子电子层结构相同 |
| C.X的气态氢化物比Y的气态氢化物稳定 |
| D.W元素的金属性比Z元素金属性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题:
其氢化物反应生成一种盐Y,A、B、C、E、F五种元素都能与D元素形成原子个数比不相同的常见化合物。回答下列问题: 充分作用后,溶液pH 7(填“>”“<”或“=”),原因是
充分作用后,溶液pH 7(填“>”“<”或“=”),原因是  。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
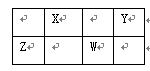
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为3 4 4 |
 键。在H-Y、H-Z两种共价键中,键的极性较强的是 ,键长较长的是 。
键。在H-Y、H-Z两种共价键中,键的极性较强的是 ,键长较长的是 。 污染的一种方法,是将其在催化剂作用下转化为单质Y。
污染的一种方法,是将其在催化剂作用下转化为单质Y。 O2(g)====XO2(g) ΔH=-283kJ·mol-1
O2(g)====XO2(g) ΔH=-283kJ·mol-1 m
m ol-1
ol-1查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com