
| A. | 金属钠形成的晶体中,每个钠原子周围与其距离最近的原子有8个 | |
| B. | 金属镁形成的晶体中,每个镁原子周围与其距离最近的原子有6个 | |
| C. | 在NaCl晶体中,每个Na+周围与其距离最近的Na+有12个 | |
| D. | 在CsCl晶体中,每个Cs+周围与其距离最近的Cl-有8个 |
分析 A、金属钠是体心立方堆积,据此判断每个钠原子周围与其距离最近的原子数;
B、金属镁是六方最密堆积,据此判断每个钠原子周围与其距离最近的原子数;
C、氯化钠晶胞中,每个钠离子周围距离最近的钠离子是12个;
D、氯化铯晶体中,铯离子的配位数是8.
解答 解:A、金属钠是体心立方堆积,钠的配位数为8,即每个钠原子周围与其距离最近的原子有8个,故A正确;
B、金属镁为六方最密堆积,堆积方式为: ,镁的配位数为12,即每个镁原子周围与其距离最近的原子有12个,故B错误;
,镁的配位数为12,即每个镁原子周围与其距离最近的原子有12个,故B错误;
C、氯化钠晶胞中,每个钠离子周围距离最近的钠离子个数=3×8÷2=12,故C正确;
D、氯化铯晶体中,铯离子的配位数是8,故D正确,
故选B.
点评 本题考查了晶体的空间结构,明确典型的晶体类型、结构、晶胞为解答本题关键,同时要求学生有丰富的空间想象能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | HCl气体溶于水形成盐酸,存在H+,所以HCl为离子化合物 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 稀有气体原子之间不易形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Ⅰ实验结果 | Ⅱ回答问题 |
| ①取原溶液少许,滴加足量氯水,产生沉淀;过滤,滤液加CCl4,振荡后,CCl4层未变色. | ①该步实验说明溶液中不存在Br-离子I-. |
| ②取原溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇空气立即变为红棕色. | ②该步实验发生反应的离子方程式为 8H++2NO3-(稀)+3Cu=3Cu2++2NO↑+4H2O. |
| ③取原溶液少许,加盐酸酸化后,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失. | ③产生白色沉淀的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+. |
| ④取原溶液少许,滴加2滴酸性高锰酸钾溶液,紫色立即褪去. | ④该步实验说明溶液中存在SO32-离子. |
| ⑤取原溶液少许,加足量Ba(NO3)2溶液产生白色沉淀,过滤;往洗涤后的沉淀中加入足量盐酸,沉淀部分溶解,有无色气体产生. | ⑤未溶解的白色沉淀是BaSO4;将气体通入品红溶液的现象是品红溶液褪色. |
| ⑥取步骤⑤所得滤液,加HNO3酸化后,再加AgNO3溶液,溶液中析出白色沉淀. | ⑥该步骤是否有意义有(填“有”或“无”). |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用含1mol FeCl3的溶液制备成Fe(OH)3胶体,其中胶粒数为NA | |
| B. | 12g金刚石中含有的共价键数为4 NA | |
| C. | 常温常压下,14 g CO和N2的混合气体中,含有原子数为NA | |
| D. | 1 L 1 mol/L NH4Cl溶液中含有NH4+数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) | |
| B. | 已知25°C时Ksp(AgCl)=1.8×10-10,则在0.1mol•L-1AgCl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10mol•L-1 | |
| C. | 0.2mol•L-1 HCl溶液与等体积0.05 mol•L-1 Ba(OH)2溶液混合后,溶液的pH=1 | |
| D. | 室温下,0.1mol•L-1NaHA溶液的pH=4,则有C(HA-)>C(H+)>C(A2-)>C(H2A) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
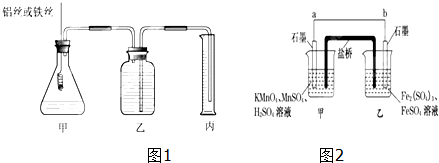
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯由于甲基对苯环的影响,导致苯环上甲基邻、对位上的氢原子易被取代而使溴水褪色 | |
| B. | 乙醇由于羟基的影响,导致乙醇甲基上的C-H键易断裂而发生消去反应生成乙烯 | |
| C. | 苯酚由于苯环的影响,导致酚羟基能与Na2CO3溶液反应生成CO2 | |
| D. | 苯酚由于羟基对苯环的影响,导致苯环上羟基邻、对位上的氢原子只能于液溴发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com