
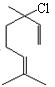
 ;
;
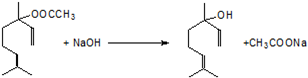 ,.
,. 分析 (1)异戊二烯和HCl发生了1,4加成生成L,L与丙酮发生取代反应生成M,M与乙炔加成生成N,N与氢气加成生成芳樟醇;
①根据K的结构简式进行命名;
②比较M和N的结构,利用元素守恒判断;
③根据L的结构简式可知,L的分子式为C5H9Cl,根据含一个甲基的条件以及书写同分异构体的方法即碳链异和官能团位置异构可判断同分异构体的种类;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为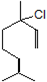 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为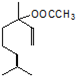 ,
, 在碱性条件下发生酯的水解得芳樟醇.
在碱性条件下发生酯的水解得芳樟醇.
解答 解:(1)异戊二烯和HCl发生了1,4加成生成L,L与丙酮发生取代反应生成M,M与乙炔加成生成N,N与氢气加成生成芳樟醇,
①根据其结构简式知其名称为2-甲基-1,3-丁二烯(或异戊二烯),故答案为:2-甲基-1,3-丁二烯(或异戊二烯);
②比较M和N的结构,利用元素守恒可知X为CH≡CH,
故答案为:CH≡CH;
③根据L的结构可知,L的分子式为C5H9Cl,L中有一个碳碳双键和一个氯原子,所以只含一个甲基的链状同分异构体可以是碳链为ClCH2=CH-CH2-CH2-CH3、ClCH2-CH2=CH2-CH2-CH3、ClCH2-CH2-CH2=CH2-CH3、CH2=CHCl-CH2-CH2-CH3、CH2=CH2-CHCl-CH2-CH3、CH2=CH2-CH2-CHCl-CH3、CH2=CH-CH(-CH3)-CH2Cl、CH2=C(-CH3)-CH2-CH2Cl、CH2=C(-CH2CH3)-CH2Cl,共有9种,
故答案为:9;
(2)月桂烯与HCl加成后再与CH3COONa反应转化为芳樟醇的乙酸酯,比较芳樟醇的结构和月桂烯的结构可知,月桂烯与一分子HCl发生加成反应,且氯原子加在芳樟醇中羟基的位置,据此可推知A的结构为 ,
, 与CH3COONa反应得B为
与CH3COONa反应得B为 ,
, 在碱性条件下发生酯的水解得芳樟醇,
在碱性条件下发生酯的水解得芳樟醇,
①通过以上分析知,A结构简式为 ,故答案为:
,故答案为: ;
;
② 在碱性条件下发生酯的水解得芳樟醇,反应方程式为
在碱性条件下发生酯的水解得芳樟醇,反应方程式为 ,
,
,故答案为: ,
,
.
点评 本题考查有机物推断,为高频考点,侧重考查学生推断能力,根据反应前后物质结构简式差异性推断反应类型或根据反应条件结合已知物质结构进行推断,难点是同分异构体种类判断,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | m=4 | B. | a=b | C. | a<$\frac{b}{2}$ | D. | m<3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
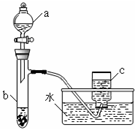 甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.
甲、乙两组同学分别对铜、铁与硝酸的反应进行探究,请你参与并完成对有关问题的解答.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2H4+O2═N2+2H2O△H=-534.4 kJ•mol-1 | |
| B. | N2H4+O2═N2+2H2O△H=-1 068.8 kJ•mol-1 | |
| C. | N2H4(g)+O2(g)═N2(g)+2H2O(g)△H=-534.4 kJ•mol-1 | |
| D. | $\frac{1}{2}$N2H4(g)+$\frac{1}{2}$O2(g)═$\frac{1}{2}$N2(g)+H2O(g)△H=+267.2 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
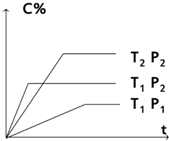 对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,
对于反应mA (g)+nB (g)?pC(g) 有如图所示的关系,查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | H2O2是氧化剂,H2O2中的氧元素被还原 | |
| B. | 每生成1 mol O2转移的电子的物质的量为2 mol | |
| C. | ClO2中的氯元素被氧化 | |
| D. | ClO2是氧化剂,H2O2是还原剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com