
��9�֣����ֶ�����Ԫ��A��B��C��D��Eԭ������������A��B��ͬһ���ڣ�A��ͬ����Ԫ���а뾶���ģ�������ϡ�����壩��Bԭ�ӵĴ�����������������������4����C��ͬ���ڼ������а뾶��С��Ԫ�أ�DԪ��ԭ�ӵ�p�����3��δ�ɶԵ��ӣ�Eԭ�ӵ�K��L�������֮�ͱ�K��M�������֮�Ͷ�1����
��1��д��EԪ�ػ�̬ԭ�ӵ���Χ�����Ų�ʽ
��2���Ƚϵ�һ�����ܵĴ�С��B C������ڡ�С�ڻ���ڣ�
��3���ֱ�д��D��E������������Ӧˮ����Ļ�ѧʽ �� �����Ƚ϶������ԣ�����ԣ���ǿ�� ������ڡ�С�ڻ���ڣ�
��4��д��B������������Ӧˮ������E������������Ӧˮ���ﷴӦ�����ӷ���ʽ
��5��д��C������������Ӧˮ������A������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽ
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
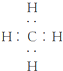
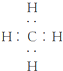
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �±����г����ֶ�����Ԫ��A��B��C��D��E����Ϣ�����ƶϺ�����
�±����г����ֶ�����Ԫ��A��B��C��D��E����Ϣ�����ƶϺ�����| Ԫ�� | �й���Ϣ |
| A | Ԫ����Ҫ���ϼ�Ϊ-2��ԭ�Ӱ뾶Ϊ0.074n m |
| B | ��������������������������֮��Ϊ4 |
| C | ԭ�Ӱ뾶Ϊ0.102n m���䵥����A�ĵ�����ȼ�գ���������������ɫ���� |
| D | ����������ˮ����ܰ�1��1�������������ȵ����������� |
| E | ԭ�Ӱ뾶Ϊ0.075n m������������ˮ���������⻯�����һ����X |
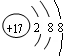
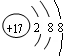


 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �й���Ϣ |
| A | Ԫ����Ҫ���ϼ�Ϊ-2��ԭ�Ӱ뾶Ϊ0.074nm |
| B | ��������������������������֮��Ϊ4��ͬ��������Ԫ����ԭ�Ӱ뾶��С |
| C | ԭ�Ӱ뾶Ϊ0.102nm���䵥����A�ĵ�����ȼ�գ���������������ɫ���� |
| D | ����������Ӧˮ����ܰ�1��1�������������ȣ�10�����ӣ����������� |
| E | ԭ�Ӱ뾶Ϊ0.075nm������������Ӧˮ���������⻯�����һ����X |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com