
| A. | 甲烷 | B. | 苯 | C. | 环己烷 | D. | 甲苯 |
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
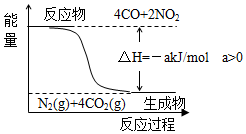 研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义.
研究NOx、SO2、CO等大气污染气体的处理方法具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热条件下,20mL10mol/L浓硝酸与足量铜反应转移电子数为0.1NA | |
| B. | 78gNa2O2固体中含有的阴离子数目为2NA | |
| C. | 标准状况下,11.2 L由CH4和C2H4组成的混合气体中含有氢原子的数目为2 NA | |
| D. | 常温下,4gCH4中含有4NA个C-H共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ③
③ ④
④
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1L0.1mol•L-1NaHCO3溶液中含有的HCO3-数目为0.1NA | |
| C. | 1LpH=1的硫酸溶液中含有的H+数为0.2NA | |
| D. | 标准状况下,2.24LCO和CO2混合气体中含有的氧原子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解CuCl2溶液,阴极析出16g铜时,电极上转移的电子数为NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | SiO2晶体中每摩尔硅原子可与氧原子形成2NA个共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | |
| B. | 相对于途径①、③,途径②更好地体现了绿色化学思想 | |
| C. | Y物质具有还原性,可以是葡萄糖 | |
| D. | 在1100℃所得混合气体X中O2一定为0.75mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com