
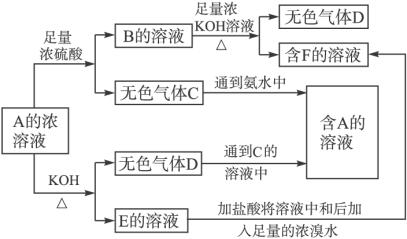
试回答:
(1)物质的化学式:
A.__________;B.__________;C.__________;
D.__________;E.__________;F.__________。
(2)写出E→F的离子方程式____________________________________。
(3)鉴定物质F的方法_______________________________________。
(1)(NH4)2SO3或NH4HSO3 (NH4)2SO4或NH4HSO4 SO2 NH3 K2SO3 K2SO4
(2)![]() +Br2+H2O====
+Br2+H2O====![]() +2Br-+2H+
+2Br-+2H+
(3)通过焰色反应鉴定K+(隔钴玻璃,火焰呈浅紫色),取少量F的溶液加入BaCl2和HNO3溶液,若有白色沉淀产生,证明![]() 的存在
的存在
解析:A盐既能与浓H2SO4反应放出气体,又能与KOH反应放出气体,说明A为具有两性的盐,即:弱酸的铵盐或者其阴离子可被氧化,再注意C、D通到相应的溶液中又生成A,说明A盐是氨与一不稳定的酸(如H2SO3、H2CO3)形成的盐,又因B是硫酸盐,与KOH反应后生成D(NH3)及硫酸钾(F),再从EF分析,E为钾盐,通入溴水后变为K2SO4,只能说明E为K2SO3,反应式![]() +Br2+H2O====
+Br2+H2O====![]() +2Br-+2H+,所以A是(NH4)2SO3或NH4HSO3。
+2Br-+2H+,所以A是(NH4)2SO3或NH4HSO3。


科目:高中化学 来源: 题型:阅读理解
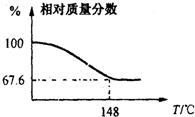 (2012?信阳一模)Na2CO3和H2O2结合成棒状晶体Na2CO3?xH2O2(过氧化氢相当于水合.Na2CO3?xH2O2同时具有Na2CO3和H2O2的性质.注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源.现称取一定质量的Na2CO3?xH2O2晶体加热.实验结果以温度和残留固体的相对质量分数示如图.
(2012?信阳一模)Na2CO3和H2O2结合成棒状晶体Na2CO3?xH2O2(过氧化氢相当于水合.Na2CO3?xH2O2同时具有Na2CO3和H2O2的性质.注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源.现称取一定质量的Na2CO3?xH2O2晶体加热.实验结果以温度和残留固体的相对质量分数示如图.查看答案和解析>>
科目:高中化学 来源: 题型:
A.NaOH B.KI C.NH3·H2O D.Na2CO3
查看答案和解析>>
科目:高中化学 来源:2012届河南省信阳市高中毕业班第一次调研考试化学试卷 题型:填空题
(16分)Na2CO3和H2O2结合成棒状晶体,Na2CO3·xH2O2(过氧化氢合相当于水合。注意:使用高浓度H2O2时一定要小心,防止爆炸生成水和氧气),可消毒、漂白或作O2源…。
现称取一定质量的Na2CO3·xH2O2晶体加热。实验结果以温度和相对质量分数示于下图。
(1)该棒状晶体的化学式Na2CO3·xH2O2中x= 。
(2)加热过程中,在141℃时表现为放热,其原因可能是:
a. Na2CO3·xH2O2分解放热
b.产生的H2O2分解放热
c. Na2CO3·xH2O2分解吸收热量小于产生的H2O2分解放出的热量
(3)事实上,Na2CO3·H2O2(x=1时)是Na2CO4·H2O(Na2CO4叫做过氧碳酸钠)。洗衣粉中加入适 量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。
量的Na2CO4可以提高洗涤质量,其目的是对衣物进行漂白、消毒。试用化学方程式表示上述洗涤原理: 。
(4)写出Na2CO4溶液与稀硫酸反应的离子方程式 。
(5)下列物质不会使过碳酸钠失效的是
| A.MnO2 | B.H2S | C.CH3COOH | D.NaHCO3 |
 。
。查看答案和解析>>
科目:高中化学 来源:湖北省模拟题 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com