
25 ��ʱ���ں���Pb2����Sn2����ij��Һ�У��������������(Sn)��������Ӧ��Sn(s)��Pb2��(aq) 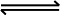 Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ��ͼ��ʾ�������ж���ȷ����(����)
Sn2��(aq)��Pb(s)����ϵ��c(Pb2��)��c(Sn2��)�仯��ϵ��ͼ��ʾ�������ж���ȷ����(����)

A����ƽ����ϵ�м������Ǧ��c(Pb2��)����
B����ƽ����ϵ�м�������Sn(NO3)2�����c(Pb2��)��С
C�������¶ȣ�ƽ����ϵ��c(Pb2��)����˵���÷�Ӧ��H>0
D��25 ��ʱ���÷�Ӧ��ƽ�ⳣ��K��2.2

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ���� | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| �е�/�� | 57.7 | 12.8 | - | 315 | - |
| �۵�/�� | -70.0 | -107.2 | - | - | - |
| �����¶�/�� | - | - | 180 | 300 | 162 |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��Դ�Ŀ����������������Ŀɳ����Է�չϢϢ��أ�
��Դ�Ŀ����������������Ŀɳ����Է�չϢϢ��أ�| 1 |
| 2 |
| ���¡���ѹ |
| ���� |
| P |
| P0 |
| O | 2- 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ӱ�ʡ��ɽ�и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
��Դ�Ŀ����������������Ŀɳ����Է�չϢϢ��ء�
I����֪��Fe2O3(s)��3C(s)= 2Fe(s)��3CO(g) ��H1=a kJ��mol-1
CO(g)��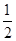 O2(g)=CO2(g)
��H2=b kJ��mol-1
O2(g)=CO2(g)
��H2=b kJ��mol-1
4Fe(s)��3O2(g)=2Fe2O3(s) ��H3=c kJ��mol-1
��C��ȼ����________kJ��mol-1
II����1������ԭ��صĹ���ԭ�������л�ѧ��Ӧ�������Ͽ�����Ƴ�ԭ��ص���____(�����)��
A��C(s)+CO2(g)=2CO(g) B��NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)
C��2H2O(l) = 2H2(g)+O2(g) D��2CO(g)+O2(g)=2CO2(g)
�������ڵ�K2CO3��CO2Ϊ��Ӧ�Ļ�����������ѡ��Ӧ��Ƴ�һ��ԭ��أ���д����ԭ��صĸ�����Ӧ��___________��
��2��ijʵ��С��ģ�ҵ�ϳɰ���ӦN2(g)��3H2(g)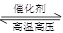 2NH3(g) ��H=-92.4kJ��mol-1����ʼ���ǽ�N2��H2�������20mol (�����1��1)����5L�ϳ����С���ӦǰѹǿΪP0����Ӧ������ѹǿ��P��ʾ����Ӧ������
2NH3(g) ��H=-92.4kJ��mol-1����ʼ���ǽ�N2��H2�������20mol (�����1��1)����5L�ϳ����С���ӦǰѹǿΪP0����Ӧ������ѹǿ��P��ʾ����Ӧ������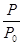 ��ʱ��t�Ĺ�ϵ��ͼ��ʾ��
��ʱ��t�Ĺ�ϵ��ͼ��ʾ��
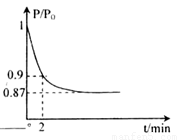
��ش��������⣺
�ٷ�Ӧ��ƽ��ı�־�ǣ�����ĸ���ţ�________��
A��ѹǿ���ֲ���
B�������ܶȱ��ֲ���
C��NH3������������N2���������ʵ�2��
��2minʱ����c(N2)�仯��ʾ��ƽ����Ӧ����Ϊ________��
�������N2��ת���ʿɲ�ȡ�Ĵ�ʩ��________��
A������ϵ�а������1��1�ٳ���N2��H2
B�������NH3
C�������¶�
D������He��ʹѹǿ����
E������һ������N2
��3��25��Cʱ��BaCO3��BaSO4���ܶȻ������ֱ���8��10��9��1��10��10��ij����BaCO3����������Һ�У�c(CO32-)=0.2mol��L-1���������������Na2SO4��Һ����Ҫ���� BaSO4����������Na2SO4��Һ�����ʵ���Ũ����С��________mol • L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�갲��ʡ��ɽ�и����ڶ�������������ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
X��Y��Z��Q��T����Ԫ��λ��ǰ�����ڣ���ԭ��������������X��Y�ĵ����ڳ��³�ѹ�³���̬��X �γɵĵ��ʷ������µ��Ӷԣ�Y�Ļ�̬ԭ����p�ܼ���������δ�ɶԵ��ӣ�Zԭ�ӵİ뾶��ͬ��������Ԫ������� Q�����������γ������һ����Ҫ���ʣ�T2+�����еĵ���������Z��Qԭ�ӵĵ�����֮�͡�
��1��QԪ��λ��Ԫ�����ڱ��� ���� �壬T2+�ĵ����Ų�ʽΪ ��
��2��YԪ�غ�QԪ�طֱ��γɵ�������Ƶ��⻯���У��е�ϸߵ��� ��д��ѧʽ����ԭ����
�ö��Ե缫���X��Y��Z����Ԫ���γɵĻ�����ˮ��Һ���������ĵ缫��ӦʽΪ ��
��3��Z��Q�γɵĻ������ˮ��Һ�� ����ԡ��������ԡ����ԡ�����ԭ��
�� �������ӷ���ʽ��ʾ����
��4����֪��25�桢101325Paʱ��
2T(s)+Q(s)=T2Q(s) ��H=-79.5KJ/mol
Q(s)+Y2(g)=QY2(g) ��H=-296.6KJ/mol
����������Ӧ����д��T2Q��Y2��Ӧ����T�� QY2���Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com