
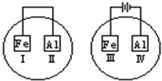
| A、II和Ⅳ | B、Ⅱ和Ⅲ |
| C、Ⅰ和Ⅲ | D、Ⅰ和Ⅳ |


科目:高中化学 来源: 题型:
| p1 |
| p2 |
| A、2:5 | B、5:2 |
| C、7:6 | D、6:7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ |
| B、OH- |
| C、S2- |
| D、C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、20mL,3 mol?L-1 |
| B、25mL,2 mol?L-1 |
| C、10mL,4 mol?L-1 |
| D、18mL,3 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 5 |
| 2 |
| A、乙炔(C2H2)的燃烧热为1256 kJ/mol |
| B、若转移10 mol电子,则消耗2.5 mol O2 |
| C、若生成2 mol液态水,则△H=-2512 kJ/mol |
| D、若形成4 mol碳氧共用电子对,则放出的热量为2512 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水在常温下属于分子晶体 |
| B、水的电离和电解都需要通电 |
| C、水分子很稳定是因为H-O共价键键能大 |
| D、金属的电化学腐蚀与水无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com