
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 根据该有机物中C、N、H原子之间都是以单键相连,以氮原子为中心,氮原子连接三个甲基;氮原子连一个氢原子、一个甲基和一个乙基;氮原子连两个氢原子和一个正丙基;氮原子连两个氢原子和一个异丙基.
解答 解:从该化合物的分子组成上可以看出,该有机物中C、N、H原子之间都是以单键相连,以氮原子为中心,氮原子连接三个甲基时是一种同分异构体,氮原子连一个氢原子、一个甲基和一个乙基时是另一种同分异构体,氮原子连两个氢原子和一个正丙基时是第三种同分异构体,氮原子连两个氢原子和一个异丙基时是第四种同分异构体,共有4种同分异构体,故选D.
点评 本题主要考查了同分异构体的判断,原子的连接方式是解题关键,难度不大,注意丙基分正丙基和异丙基.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHSO4 和 Ba(OH)2 | B. | NaAlO2和HCl | C. | Na2CO3和 HCl | D. | AlCl3和 NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1(b-2a)mol•L-1 | B. | 10(2a-b)mol•L-1 | C. | 10(b-a)mol•L-1 | D. | 10(b-2a)mol•L -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
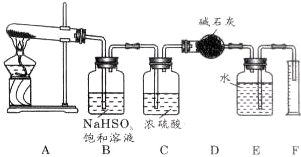
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol醋酸的质量与NA个醋酸分子的质量相等 | |
| B. | NA个氧气分子和NA个氢气分子的质量比等于16:1 | |
| C. | 30g乙烷(C2H6)所含的原子数目为NA | |
| D. | 在标准状况下,0.5NA个氯气分子所占体积约是11.2L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
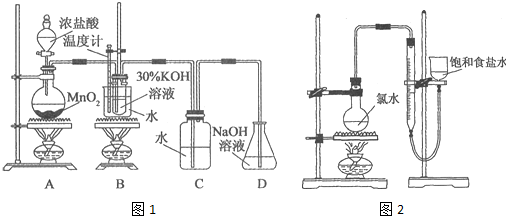
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.2mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水/mL | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com