
 工业利用上述信息,按图所示的路线合成物质M(结构简式如右图所示),该物质是一种香料.
工业利用上述信息,按图所示的路线合成物质M(结构简式如右图所示),该物质是一种香料.
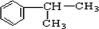 可与氯气发生取代反应生成
可与氯气发生取代反应生成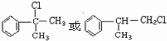 ,B能发生加成反应,则A应发生消去反应,B为
,B能发生加成反应,则A应发生消去反应,B为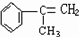 ,根据产物可知D为
,根据产物可知D为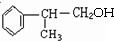 ,则C为
,则C为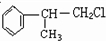 ,以此解答该题.
,以此解答该题.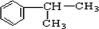 可与氯气发生取代反应生成
可与氯气发生取代反应生成 ,B能发生加成反应,则A应发生消去反应,B为
,B能发生加成反应,则A应发生消去反应,B为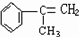 ,根据产物可知D为
,根据产物可知D为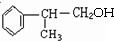 ,则C为
,则C为 ,
, ,
,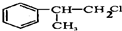 (或
(或 );
);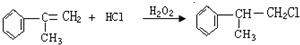 ,
,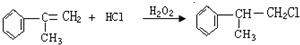 ;
;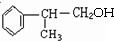 ,D和浓硫酸共热发生消去反应的化学方程式为
,D和浓硫酸共热发生消去反应的化学方程式为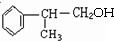
| 浓硫酸 |
| △ |
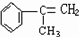 +H2O,
+H2O,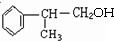
| 浓硫酸 |
| △ |
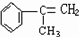 +H2O;
+H2O; ,
, (其中之一).
(其中之一).


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 .化合物
.化合物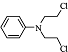 是合成抗癌药物美发伦的中间体,现以
是合成抗癌药物美发伦的中间体,现以 和
和 为原料制备该化合物的合成路线流程图如下,请在空白处填写相应的有机物的结构简式.
为原料制备该化合物的合成路线流程图如下,请在空白处填写相应的有机物的结构简式.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属钠要保存在煤油中 |
| B、金属铝的熔点高,常作为耐高温的材料 |
| C、氢氧化亚铁是白色絮状沉淀,在空气中变成灰绿色,最终会变成红褐色 |
| D、小苏打、氢氧化铝都可以治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 一定条件 |

 (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化) 与浓硫酸、浓硝酸混合,在不同温度下会得到不同产物.
与浓硫酸、浓硝酸混合,在不同温度下会得到不同产物.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入Al能放出H2的溶液中:Fe2+、Al3+、NO3-、Cl- |
| B、使酚酞显红色的溶液中:Na+、AlO2-、NO3-、HSO3- |
| C、在无色溶液中:K+、Ca2+、SO32-、Cl- |
| D、加入Mg能放出H2的溶液中:NH4+、Cl-、K+、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com