
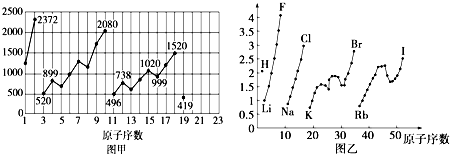
| A、图甲可能表示的是元素原子的第一电离能随原子序数的变化关系 |
| B、图甲可能表示的是元素单质的熔点随原子序数的变化关系 |
| C、图乙可能表示的是元素原子的半径随原子序数的变化关系 |
| D、图乙不可能表示元素的电负性随原子序数的变化关系 |


科目:高中化学 来源: 题型:
| A、通CO的一极是电池的正极 |
| B、负极电极反应是:O2+2CO2+4e-=2CO32- |
| C、熔融盐中CO32-的物质的量在工作时保持不变 |
| D、正极发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| X | 白色沉淀 | 白色沉淀 | 白色沉淀 | 无现象 |
| 稀硝酸 | 沉淀不消失 | 沉淀消失 有气体产生 | 沉淀不消失 | 无现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)实验室一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样.为了确定该固体的成分,可以选择下列
(1)实验室一瓶固体M的标签右半部分已被腐蚀,剩余部分只看到“Na2S”字样.为了确定该固体的成分,可以选择下列查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、110g |
| B、110g/mol |
| C、55g/mol |
| D、55 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1个甘氨酸分子中存在10对共用电子 |
| B、PCl3和了BCl3分子中所有原子的最外层都达到8电子稳定结构 |
| C、维勒用无机物合成了尿素,突破了无机物与有机物的界限 |
| D、熔点由高到低的顺序是:金刚石>碳化硅>晶体硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com