
 ;
;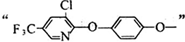
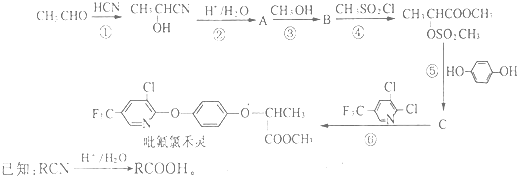
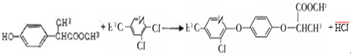
分析 由反应信息可知,CH3CH(OH)CN在酸性条件下发生水解反应生成A,A为CH3CH(OH)COOH,与CH3OH发生正反应生成B,B为CH3CH(OH)COOCH3.C与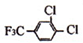 反应生成毗氟氯禾灵,结合毗氟氯禾灵的结构及生成C的反应物可知,C为
反应生成毗氟氯禾灵,结合毗氟氯禾灵的结构及生成C的反应物可知,C为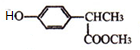 ,在上述流程中,反应①属于加成反应,反应②属于水解反应,反应③④⑤⑥属于取代反应,据此答题.
,在上述流程中,反应①属于加成反应,反应②属于水解反应,反应③④⑤⑥属于取代反应,据此答题.
解答 解:由反应信息可知,CH3CH(OH)CN在酸性条件下发生水解反应生成A,A为CH3CH(OH)COOH,与CH3OH发生正反应生成B,B为CH3CH(OH)COOCH3.C与 反应生成毗氟氯禾灵,结合毗氟氯禾灵的结构及生成C的反应物可知,C为
反应生成毗氟氯禾灵,结合毗氟氯禾灵的结构及生成C的反应物可知,C为 ,在上述流程中,反应①属于加成反应,反应②属于水解反应,反应③④⑤⑥属于取代反应,
,在上述流程中,反应①属于加成反应,反应②属于水解反应,反应③④⑤⑥属于取代反应,
(1)根据上面的分析可知,A为CH3CH(OH)COOH,A中含有的所有官能团的名称为羟基和羧基,
故答案为:羟基和羧基;
(2)根据上面的分析可知,反应①~⑥中,属于加成反应的有①,
故答案为:①;
(3)B为CH3CH(OH)COOCH3,
故答案为:CH3CH(OH)COOCH3;
(4)C为 ,分子中的酚羟基和酯基都与氢氧化钠反应,所以1mol有机物C与足量的NaOH溶液充分反应,最多可消耗2mol NaOH,
,分子中的酚羟基和酯基都与氢氧化钠反应,所以1mol有机物C与足量的NaOH溶液充分反应,最多可消耗2mol NaOH,
故答案为:2;
(5)反应⑥的化学方程式为 ,
,
故答案为: ;
;
(6)吡氟氯禾灵的同分异构体,同时满足下列两个条件①含有 ,②能与碳酸氢钠溶液反应生成二氧化碳,说明有羧基,符合条件的结构有
,②能与碳酸氢钠溶液反应生成二氧化碳,说明有羧基,符合条件的结构有 上连有-CH2CH2CH2COOH、-CH(CH3)CH2COOH、-CH2CH(CH3)COOH、-C(CH3)2COOH、-CH(CH2CH3)COOH,共有5种,
上连有-CH2CH2CH2COOH、-CH(CH3)CH2COOH、-CH2CH(CH3)COOH、-C(CH3)2COOH、-CH(CH2CH3)COOH,共有5种,
故答案为:5.
点评 本题考查有机物的推断和合成,题目较为综合,难度中等,注意利用题中信息和正推、逆推相结合进行推断,是热点题型,需要学生熟练掌握官能团的性质与转化.


科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①③④ | C. | ③④⑤ | D. | ④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加水稀释,电离平衡正向移动,溶液中n(H+)减小 | |
| B. | 加热,电离平衡正向移动,溶液中c(CH3COO-)增大 | |
| C. | 通入少量HCl气体,电离平衡逆向移动,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,电离平衡逆向移动,溶液中c(H+)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
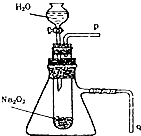 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C6H12,分子结构中含有3个“-CH3”原子团的烯烃共有 5种 | |
| B. | 芥子醇(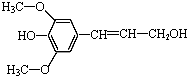 ) 能发生氧化、取代、水解、加聚反应 ) 能发生氧化、取代、水解、加聚反应 | |
| C. | 实验室制乙烯时,把生成的气体通入酸性KMnO4溶液,紫色褪去,不能说明一定生成了乙烯 | |
| D. | 将少量某物质的溶液滴加到新制银氨溶液中,水浴加热后有银镜生成,该物质不一定属于醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ).
).
 .
. .
. .
. 、
、 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题


| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
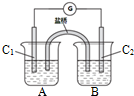 已知砷(As)元素的原子结构示意图为
已知砷(As)元素的原子结构示意图为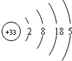
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com