
| A、饱和NH4Cl溶液中:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| B、0.1mol/LNaHCO3溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L |
| C、饱和NaHS溶液中:c(Na+)>c(HS-)>c(H+)>c(OH-) |
| D、0.1mol/LCH3COONa溶液中:c(CH3COO-)>c(OH-) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3- |
| B、若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 |
| C、若向该溶液中加人过量的稀硫酸和KSCN溶液,溶液显血红色 |
| D、若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所得溶液中阳离子和阴离子的物质的量之比为1:2 |
| B、反应中消耗的水的质量是加入的Al的质量的2倍 |
| C、所得溶液中Na+和Al3+的物质的量之比为2:1 |
| D、反应中放出的气体在标准状况下的体积为2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:
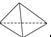 .下列说法不正确的是( )
.下列说法不正确的是( )| A、白磷着火点低,在空气中可自燃 |
| B、白磷、红磷互为同素异形体 |
| C、31g白磷中,含P-P键1.5 mol |
| D、已知P4(白磷,s)+3O2(g)═2P2O3(s)△H=-Q kJ?mol-1,则白磷的燃烧热为Q kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯的分子式:CH2═CH2 |
| B、次氯酸分子的结构式:H-O-Cl |
C、羟基的电子式: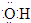 |
| D、以铁作阳极电解时,阳极的电极反应式:Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com