
| A、NH4+、Al3+、SO42-、NO3- |
| B、Ba2+、K+、Cl-、SO42- |
| C、K+、MnO4-、NH4+、NO3- |
| D、Mg2+、K+、CO32-、NO3- |


科目:高中化学 来源: 题型:
A、饱和溶液的物质的量浓度为C=
| ||
B、饱和溶液中溶质的质量分数为W=
| ||
C、25℃时R的溶解度为S=
| ||
D、饱和溶液的密度为ρ=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行分液,分液漏斗中的下层液体从下端流出,上层则从上口倒出 |
| B、萃取,分液前需对分液漏斗检漏 |
| C、为保证分液漏斗内的液体顺利流下,需将上口塞子打开或凹槽对准小孔 |
| D、用酒精萃取溴水中的溴单质的操作可以选用分液漏斗,振荡后静置分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10ml 1.5mol/L AlCl3溶液 |
| B、100ml 1mol/L KCl溶液 |
| C、50ml 3mol/L NH4Cl溶液 |
| D、100ml 0.5mol/L MgCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、n(Cl2):n(Fe)=5:4 5Cl2+4Fe
| ||||
| B、n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | ||||
| C、n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | ||||
| D、n(Fe):n(HNO3(稀))═1:3 4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| △ |

| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
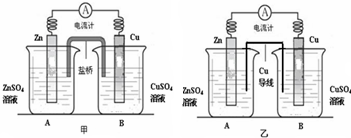
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| t(°C) | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.59 | 0.38 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com