
【题目】苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是
A. 与液溴混合后加入铁粉可发生取代反应
B. 能使酸性高锰酸钾溶液褪色
C. 1 mol苯乙烯最多能消耗2.5 molH2
D. 在催化剂存在下可以制得聚苯乙烯
科目:高中化学 来源: 题型:
【题目】下列关于氯气的实验装置能达到实验目的或实验效果的是( ) 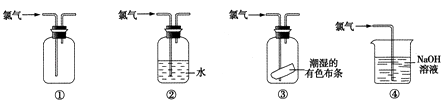
①可用于氯气的收集
②可用于除去氯气中少量的氯化氢气体
③可证明氯气具有漂白性
④可用于实验室氯气的尾气吸收.
A.①②
B.①③
C.②③
D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A和气体甲、乙、丙及物质B,C,D,E,F,G,它们之问能发生如下反应,其中乙是黄绿色气体(图中有些反应的产物和反应的条件没有全部标出). 
请根据以上信息回答下列问题:
(1)写出下列物质的名称:丙;
(2)写出下列物质的化学式:F;
(3)气体乙是一种重要的化工原料,在工农业牛产、牛活中有着重要的应用.请你根据所学知识回答下列问题:
①把气体乙通入紫色石蕊溶液中,可以观察到的现象是: , 请你解释其中的原因 .
②某化学兴趣小组计划用气体乙和物质B制取简易消毒液D.其反应原理为:(用化学方程式表示) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是( )
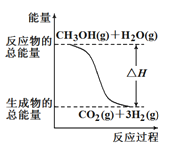
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ/mol
根据上述反应,下列说法正确的是
A.右图表示反应①中的能量变化
B.可推知2H2(g)+O2(g)=2H2O(g) ΔH=-483.8 kJ/mol
C.1 mol CH3OH充分燃烧放出的热量为192.9 kJ
D.CH3OH转变成H2的过程一定要吸收能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 芳香烃(即含苯环的烃)的获取主要来自煤的干馏和对石油分馏产品的催化重整
B. 正丁烷转化为异丁烷一定有能量变化
C. 石油的催化裂化主要目的是提高轻质液体燃料的产量尤其是汽油的产量
D. 石油的催化裂解是为了能得到润滑油、石蜡等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在已经处于化学平衡状态的体系中,如果下列量发生变化,其中一定能表明化学平衡移动的是
A. 反应混合物的浓度 B. 反应物的转化率
C. 正、逆反应的速率 D. 反应体系的压强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)对于下列反应:2SO2+O2![]() 2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为,用O2浓度变化来表示的反应速率为。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为,用O2浓度变化来表示的反应速率为。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
(2)下图左表示在密闭容器中反应:2SO2+O2![]() 2SO3 △H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;若增大压强时,反应速率变化情况画在c~d处.
2SO3 △H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是 ;bc过程中改变的条件可能是 ;若增大压强时,反应速率变化情况画在c~d处.

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列示意图与对应的反应情况正确的是
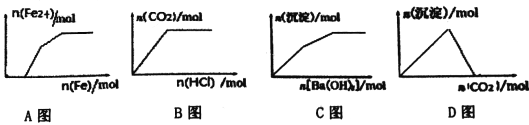
A. Fe(NO3)3、Cu(NO3)2、HNO3混合溶液中逐渐加入铁粉
B. Na2CO3、NaHCO3溶液中逐滴加入HCl
C. KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
D. NaAlO2溶液中逐渐通入CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com